このページのまとめ
- pHは水素イオン(H⁺)の濃度を基にして、溶液の酸性や塩基性を示す指標。
- pHが7より低いと酸性、7より高いと塩基性、7が中性である。
- pHは化学反応や生物活動に影響を与え、適切に管理することが重要。
- pHはpH試験紙やpHメーターを使って測定する。
~先生と生徒の会話~
 生徒
生徒pHの話を聞いたことはあるんですが、何を意味しているのかがちょっと曖昧です。pHってどうやって決まるんですか?



pHというのは、溶液の酸性や塩基性を示す指標の一つなんだ。具体的には、水素イオン(H⁺)の濃度を基にして、溶液が酸性か塩基性かを数値で表しているんだよ。pHは次の式で計算されるんだ。
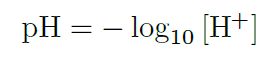
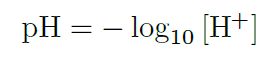



この式が示すように、pHの値は水素イオンの濃度が高いと低くなり、濃度が低いと高くなる。つまり、pHが7より低ければ酸性、7より高ければ塩基性ということになるんだ。



ああ、だからpHが1とか2だと強い酸、逆にpHが12とか13だと強い塩基になるんですね!じゃあ、pHが7だと中性ってことですか?



その通り!pHが7のときは中性で、これは純水のpH値だよ。水はわずかに電離してH⁺とOH⁻(水酸化物イオン)に分かれているけど、その量が極めて少ないため、pHが7になるんだ。中性の水では、H⁺の濃度とOH⁻の濃度がちょうど釣り合っているから、酸性でも塩基性でもない状態なんだよ。溶液中で成立するH⁺とOH⁻の関係を水のイオン積といい、25℃で1.0×10-14という数値を示すよ。この関係は水溶液の中で常に成立しているんだ。
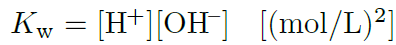
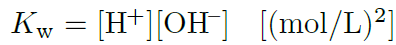



でも、pHはただの数値に見えるけど、なぜそんなに重要なんですか?



pHが重要なのは、化学反応や生物の活動に大きく関わっているからだね。例えば、人体の血液のpHは7.4程度で、この範囲を少しでも外れると体に重大な影響が出てしまうんだ。だから、体内ではpHを一定に保つために「緩衝液」という仕組みが働いているんだよ。



また、工業的にもpHの管理はとても重要で、例えば化学工場では反応の効率を最適に保つためにpHを厳密に調整しているんだ。pHがずれると、思わぬ副産物ができたり、反応が進まなかったりすることがあるんだよ。



なるほど!pHを管理することで、反応をコントロールできるんですね。でも、どうやってpHを実際に測るんですか?



pHを測るには、いくつかの方法があるんだ。一番手軽なのは「pH試験紙」を使う方法だね。この紙に溶液をつけると、その溶液のpHに応じて色が変わるんだ。変化した色を基準表と照らし合わせて、pHをざっくりと測定できるんだよ。



もっと精密な測定が必要な場合は、「pHメーター」という装置を使うことがある。この装置は電極を使って溶液中のH⁺の濃度を直接測定するから、非常に正確な値を知ることができるんだ。



pHメーターって理科室でも見たことがあります!あれでpHを測ると、どんな溶液でもすぐに数値がわかるんですね。でも、酸や塩基が混ざるとpHはどう変わるんですか?



酸や塩基が溶液に加わると、そのpHは大きく変わるよ。例えば、酸を加えるとH⁺の濃度が増えるから、pHは低くなって酸性が強くなる。逆に、塩基を加えるとOH⁻の濃度が増えてH⁺が減るので、pHは高くなって塩基性が強くなるんだ。これを利用して、酸や塩基を加えて溶液のpHを調整することがよく行われるんだよ。
例題&解答
【例題1】
次の溶液のpHを計算しなさい。
水素イオン濃度:[H⁺] = 1.0 × 10⁻⁴ mol/L
【解答】
pH = -log [H⁺]
pH = -log (1.0 × 10⁻⁴) = 4
【例題2】
pHが3の溶液に酸を加えた場合、pHはどのように変化するか説明しなさい。
【解答】
酸を加えることでH⁺の濃度が増加するため、pHはさらに低くなり、酸性が強まる。













