このページのまとめ
- 電池は、化学反応(酸化還元反応)を使って電気を作る装置。負極で酸化、正極で還元が起こる。
- 電気分解は、電気を使って化学反応を引き起こすプロセス。逆に、電気エネルギーを使って物質を分解したり、新しい物質を作ったりする。
~先生と生徒の会話~
 生徒
生徒電池って、日常的に使っているけど、実際どういう仕組みで電気を生み出しているんですか?



電池は、化学反応を使って電気を生み出す装置なんだ。具体的には、電池の中で酸化還元反応が起きているんだよ。電池には2つの電極、つまり正極と負極があって、負極では金属が酸化されて電子を放出し、その電子が外部回路を通って正極に移動するんだ。このとき、電流が流れるんだよ。そして正極では、電子を受け取った物質が還元されることで、電池として電気を供給するんだ。
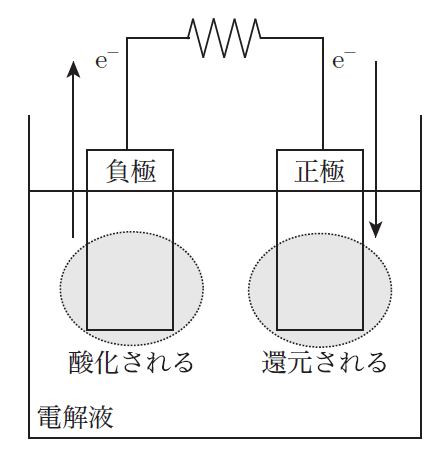




酸化還元反応を利用しているんですね!じゃあ、電池の中では具体的にどんな反応が起こっているんですか?



例えば、アルカリ乾電池を例にとると、負極側では亜鉛(Zn)が酸化されて電子を放出するんだ。具体的には、Zn → Zn²⁺ + 2e⁻という反応が起こっている。一方、正極では酸化マンガン(MnO₂)が電子を受け取って還元されるんだ。これによって、電流が生まれるんだよ。要するに、金属の酸化・還元の反応を利用して、電気エネルギーを生み出しているんだ。



なるほど!電気が流れる仕組みがよくわかりました。ところで、電気分解って電池とどう違うんですか?



電気分解は、電池とは逆の現象なんだ。電池では化学エネルギーを電気に変えているけど、電気分解では電気を使って化学反応を起こしているんだよ。例えば、水の電気分解では、水に電流を流すことで、水分子(H₂O)を水素と酸素に分解するんだ。
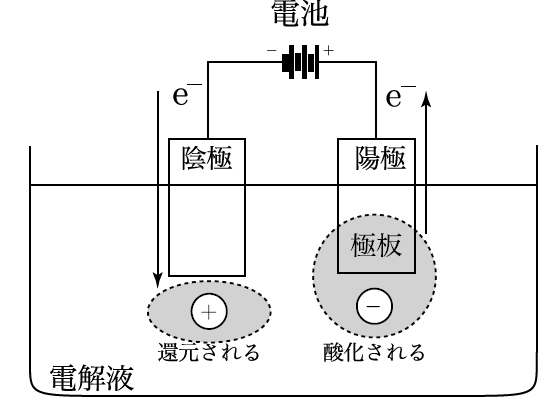




電気を使って化学反応を起こすんですね!具体的な例を教えてください。



一つの例として、塩化ナトリウム(NaCl)の電気分解があるよ。溶融塩を電気分解すると、陽極では塩化物イオン(Cl⁻)が電子を放出して塩素ガス(Cl₂)を生成し、陰極ではナトリウムイオン(Na⁺)が電子を受け取って金属ナトリウム(Na)として析出するんだ。このように、電気分解では、電気を使って化学結合を切ったり、新しい物質を生成したりできるんだよ。



電気を使って物質を分解して新しいものを作るんですね!電池と電気分解は、逆のプロセスを使っているんですね。



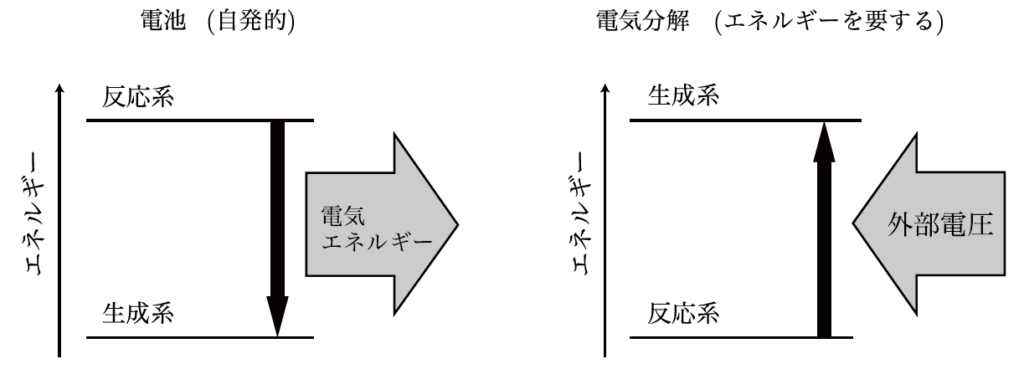
その通りだね。電池は、化学反応を使って電気を作り出し、電気分解はその逆で、電気を使って化学反応を引き起こすんだ。この仕組みを理解することで、私たちはエネルギーを効率よく使う方法を学べるんだよ。たとえば、電池で蓄えた電気を利用して電気分解を行い、新しい物質を作り出すこともできるんだ。

例題&解答
【例題1】
電池の原理において、負極側で起こる酸化反応の一例を示しなさい。
【解答】
Zn → Zn²⁺ + 2e⁻
【例題2】
水の電気分解で発生する2つの気体を答えなさい。
【解答】
水素(H₂)と酸素(O₂)











