このページのまとめ
- 燃料電池は、水素と酸素を使って電気を作り、排出物は水だけというクリーンなエネルギー源。
- 酸型(PEFC)と塩基型(AFC)の2種類があり、電解質としてプロトン(H⁺)と水酸化物イオン(OH⁻)が移動する違いがある。
- 酸型燃料電池は効率が高いが、コストが高い。塩基型燃料電池はコストが低いが、水素の純度に敏感。
- それぞれの燃料電池が、電気自動車や住宅用発電システムで活用されている。
~先生と生徒の会話~
 生徒
生徒燃料電池って、最近話題になっているけど、どんな仕組みで電気を作っているんですか?水素を使うって聞いたけど、詳しく教えてください。



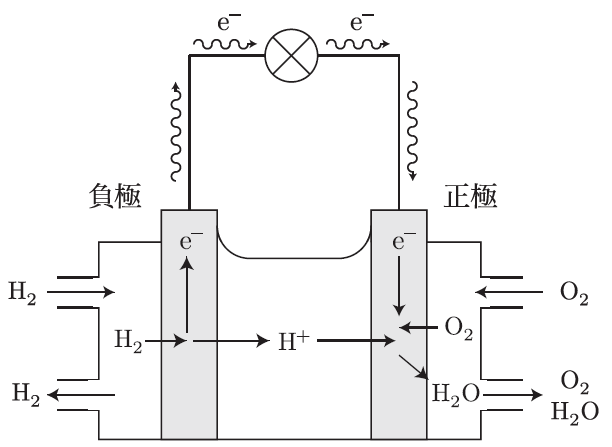
燃料電池は、水素と酸素を使って電気を生み出す装置なんだ。簡単に言うと、水素を燃料として使って、酸素と反応させることで電気を作り、その過程で生成されるのは水だけ。だから、クリーンなエネルギー源として注目されているんだよ。例えば、一般的な酸型燃料電池(PEFC)では、次のような化学反応が起こっているんだ。



水素の酸化(負極側):2H₂ → 4H⁺ + 4e⁻
酸素の還元(正極側):O₂ + 4H⁺ + 4e⁻ → 2H₂O



水素が酸化されてH⁺(プロトン)になり、電子が外部回路を通って酸素に渡り、酸素が還元されることで水ができるんだよ。




水だけができるんですね!環境にすごく良さそうですね。



その通り。燃料電池は、二酸化炭素(CO₂)を排出しないため、温暖化の原因にもならないクリーンなエネルギー源だよ。これが、電気自動車や家庭用発電システムに使われている理由なんだ。



でも、燃料電池にはいくつか種類があるって聞いたんですけど、どう違うんですか?



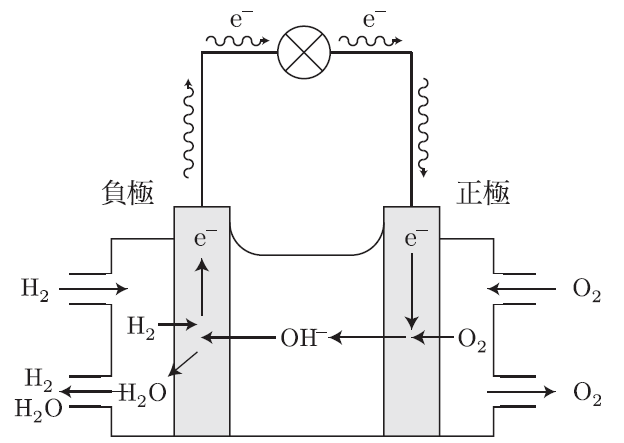
主な違いは使っている電解質だね。今話した酸型燃料電池(PEFC)では、プロトンが移動するんだけど、塩基型の燃料電池(AFC)では、OH⁻(水酸化物イオン)が移動するんだ。塩基型燃料電池では、次のような反応が起こっているよ。



水素の酸化(負極側):H₂ + 2OH⁻ → 2H₂O + 2e⁻
酸素の還元(正極側):O₂ + 2H₂O + 4e⁻ → 4OH⁻



酸型と違って、塩基型ではOH⁻がイオンとして移動するんだ。だから、正極と負極での反応が少し違うけど、基本的には水素と酸素を使って電気を作るという点は共通しているんだよ。




OH⁻が移動するんですね。じゃあ、酸型と塩基型のメリットやデメリットって何かあるんですか?



酸型燃料電池は、水素を使う際の効率が高いけど、貴金属(例えば白金)を触媒として使わなければならないため、コストが高いというデメリットがあるんだ。一方、塩基型燃料電池は触媒に貴金属を使わないで済むことが多いから、コストを抑えられる可能性があるんだ。ただし、塩基型は水素の純度に敏感で、不純物が混ざると効率が下がるという問題があるんだよ。



なるほど、それぞれにメリットと課題があるんですね。最近はどっちが多く使われているんですか?



現状では、酸型燃料電池(PEFC)の方が主流だよ。車や住宅用の燃料電池は、この酸型が多いんだ。ただ、今後は技術の進化に伴って、塩基型ももっと普及するかもしれないね。コスト削減や効率向上が進めば、さまざまな用途に使われる可能性があるんだ。



技術の進歩によって、燃料電池もこれからどんどん進化しそうですね!もっといろんな場面で使われるようになると、環境に良い影響を与えそうです。



そうだね。燃料電池が普及すれば、クリーンエネルギーの供給源として社会全体の二酸化炭素排出量を大幅に減らすことができるかもしれない。今後のエネルギー技術の発展が楽しみだね。
例題&解答
【例題1】
塩基型燃料電池で、負極側で起こる反応式を示しなさい。
【解答】
H₂ + 2OH⁻ → 2H₂O + 2e⁻
【例題2】
酸型燃料電池と塩基型燃料電池の違いを説明しなさい。
【解答】
酸型燃料電池では、H⁺(プロトン)が電解質として移動し、貴金属触媒が必要。塩基型燃料電池では、OH⁻(水酸化物イオン)が移動し、触媒に貴金属を使わない場合が多いが、水素の純度に敏感である。











