このページのまとめ
- 金属イオンの分離では、沈殿反応、pH調整、錯イオン形成、溶解度の違いを使います。
- 沈殿反応では、特定の金属イオンが試薬と反応して沈殿を作り、pH調整では酸性・アルカリ性の条件で異なる金属を分けます。
- 錯イオン形成では配位子を使って金属イオンを溶液中に保つことができ、溶解度の違いを利用して金属を分ける方法もあります。
~先生と生徒の会話~
 生徒
生徒金属イオンの分離って、どんなときに使われるんですか?



金属イオンの分離は、いろいろな金属が混ざった水溶液から、特定の金属イオンだけを取り出したいときに使われるんだ。例えば、分析化学で金属イオンの種類を特定したり、有害な金属を取り除くための環境処理にも使われるんだよ。金属イオンごとに性質が異なるから、その違いを利用して順番に分離していくんだ。




どんな性質の違いを利用して分けるんですか?



たとえば、ある金属イオンだけが特定の条件で沈殿を作るとか、pHの違いで反応が変わるとか、そんな化学的な性質を使うんだよ。あとは、錯イオンという特殊な結合を利用して、金属イオンを溶液中に残したまま他の金属を取り出す方法もあるんだ。



沈殿を使った分離って、どうやるんですか?



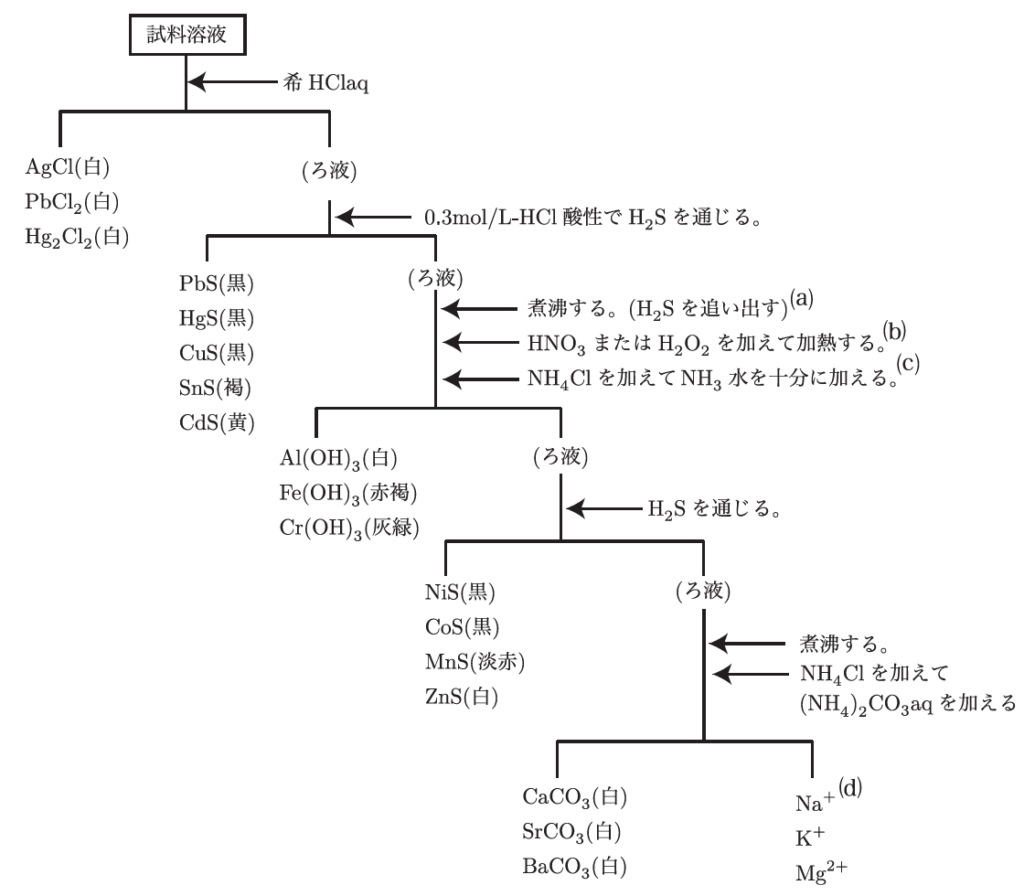
沈殿反応を使う場合、特定の試薬を加えて金属イオンと反応させ、固体の沈殿を作らせるんだ。たとえば、塩酸(HCl)を加えると、銀イオン(Ag⁺)や鉛イオン(Pb²⁺)がそれぞれ塩化物の沈殿を作るんだ。



反応式としては、Ag⁺ + Cl⁻ → AgCl↓やPb²⁺ + 2Cl⁻ → PbCl₂↓という感じだね。銀や鉛は沈殿するけれど、他の多くの金属イオンは溶液に残るから、こうして順番に分離できるんだ。



なるほど、金属ごとに沈殿を作らせるんですね。他にはどんな分離法があるんですか?



硫化物沈殿もよく使われるんだよ。たとえば、酸性の溶液に硫化水素(H₂S)を加えると、銀(Ag⁺)や銅(Cu²⁺)のような金属イオンが硫化物として沈殿するんだ。反応式は、Ag⁺ + S²⁻ → Ag₂S↓やCu²⁺ + S²⁻ → CuS↓こんな感じで、硫化銀や硫化銅の沈殿ができるんだ。



でも、pHがアルカリ性だと亜鉛(Zn²⁺)や鉄(II)(Fe²⁺)も硫化物を作るから、pHを調整することで金属を順番に分けることができるんだよ。



じゃあ、pHを使った分離もあるんですね?



そうだね。たとえば、アルミニウム(Al³⁺)は、弱アルカリ性で水酸化アルミニウム(Al(OH)₃)の沈殿を作るんだ。
反応式は、Al³⁺ + 3OH⁻ → Al(OH)₃↓という感じだね。



一方、亜鉛(Zn²⁺)はアルカリ性だと沈殿せずに、テトラヒドロキシ亜鉛酸イオン([Zn(OH)₄]²⁻)として溶けたままになるんだ。だから、pHを少しずつ変えながら、金属ごとに違うタイミングで沈殿させていくことで、順番に分離できるんだよ。



錯イオンを使った分離もあるって言っていましたよね?



うん、錯イオンの形成も大事な分離法だよ。たとえば、銅(II)イオン(Cu²⁺)にアンモニア(NH₃)を加えると、テトラアンミン銅(II)イオン [Cu(NH₃)₄]²⁺ができるんだ。



反応式は、Cu²⁺ + 4NH₃ → [Cu(NH₃)₄]²⁺という感じだね。この錯イオンは水溶液中に溶けたままになるから、他の金属を沈殿させて銅だけを分離できるんだ。こうやって、金属の錯イオン形成能力を利用して、特定の金属だけを選んで残すことができるんだよ。



すごいですね。溶解度の違いも使った分離法があるんですか?



その通りだよ。金属イオンを特定の化合物に変えて、その溶解度の違いを使って分離することもあるんだ。たとえば、バリウム(Ba²⁺)やカルシウム(Ca²⁺)は硫酸イオン(SO₄²⁻)と反応して、それぞれ硫酸バリウム(BaSO₄)や硫酸カルシウム(CaSO₄)の沈殿を作るんだ。



反応式としては、Ba²⁺ + SO₄²⁻ → BaSO₄↓やCa²⁺ + SO₄²⁻ → CaSO₄↓という感じだね。こうやって、特定の硫酸塩だけが沈殿するタイミングを利用して金属を分離するんだ。
例題&解答
【例題1】
銀イオン(Ag⁺)と鉛イオン(Pb²⁺)を塩酸で分離する際の反応を説明しなさい。
【解答】
塩酸を加えることで、銀イオンと鉛イオンはそれぞれ塩化物の沈殿を作ります。
反応式:Ag⁺ + Cl⁻ → AgCl↓ Pb²⁺ + 2Cl⁻ → PbCl₂↓
【例題2】
銅(II)イオン(Cu²⁺)をアンモニアで溶液中にとどめるための錯イオン形成の反応を説明しなさい。
【解答】
アンモニアを加えると、銅(II)イオンはテトラアンミン銅(II)イオンを形成し、溶液中に溶けたままになります。
反応式:Cu²⁺ + 4NH₃ → [Cu(NH₃)₄]²⁺