このページのまとめ
- 鉛蓄電池は、鉛と酸化鉛を使った二次電池で、充電・放電を繰り返せる。
- 負極では鉛が硫酸鉛に変わり、正極では酸化鉛が硫酸鉛に変わることで放電が進む。
- 塩橋や素焼き板は使用されず、単一の硫酸溶液で反応が行われる。
- 改良型の鉛蓄電池には、密閉型などがあり、効率が向上している。
~先生と生徒の会話~
 生徒
生徒鉛蓄電池ってどういう電池なんですか?名前は聞いたことがありますが、仕組みがよくわからなくて…。



鉛蓄電池は、充電可能な「二次電池」の一種で、車のバッテリーなどに使われているんだ。二次電池というのは、一度使い終わっても充電することで再利用できる電池のことだよ。鉛蓄電池では、鉛(Pb)と酸化鉛(PbO₂)が電極として使われ、硫酸(H₂SO₄)の電解液で反応が進むことで電流が発生するんだ。この反応は、電気を使って充電することでも逆に進行して、再びエネルギーを蓄えることができるんだよ。




二次電池なんですね!じゃあ、電気を蓄えたり、放出したりする反応がどんな風に進んでいるんですか?



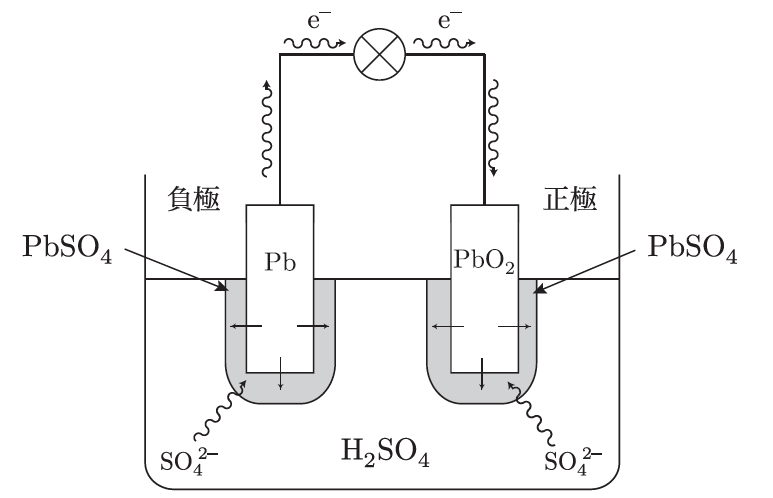
鉛蓄電池では、放電中に次のような反応が起こるんだ。まず、負極の鉛(Pb)は、硫酸イオン(SO₄²⁻)と反応して硫酸鉛(PbSO₄)を生成しながら、電子を放出する。一方、正極の酸化鉛(PbO₂)も同様に硫酸イオンと反応して硫酸鉛を生成し、電子を受け取るんだ。このようにして、電子が外部回路を通じて流れ、電流が発生するんだよ。



具体的な反応式を示すと、こうなるんだ:



負極(鉛): Pb + SO₄²⁻ → PbSO₄ + 2e⁻



正極(酸化鉛): PbO₂ + SO₄²⁻ + 4H⁺ + 2e⁻ → PbSO₄ + 2H₂O



このとき、放電が進むにつれて、両方の電極でPbSO₄が生成され、電池のエネルギーが減少していくんだ。



鉛が硫酸鉛に変わるんですね!でも、どうやって再び充電するんですか?



充電する際には、放電時の反応を逆方向に進めるんだ。電流を流すことで、鉛と酸化鉛を再び生成し、エネルギーを蓄えるんだ。充電時の反応式は次のようになる:



負極: PbSO₄ + 2e⁻ → Pb + SO₄²⁻



正極: PbSO₄ + 2H₂O → PbO₂ + SO₄²⁻ + 4H⁺ + 2e⁻



充電の結果、再び鉛と酸化鉛ができるので、電池として再利用できるんだよ。これが鉛蓄電池の強みで、何度も充電して使えるから、特に車のバッテリーとしてよく使われているんだ。



再び鉛と酸化鉛ができることで、エネルギーを蓄えられるんですね!でも、鉛蓄電池に塩橋や素焼き板は使われているんですか?



鉛蓄電池では塩橋や素焼き板は使われていないんだ。これらは主に、ダニエル電池などで使われる部品で、溶液の混合を防いでイオンの移動を制御するために用いられるんだ。でも、鉛蓄電池は1種類の電解液(硫酸)を使っているから、塩橋や素焼き板のような仕組みは必要ないんだよ。



鉛蓄電池は仕組みが少し違うんですね!でも、鉛蓄電池の改良型とかもあるんですか?



そうだね、鉛蓄電池もいろいろと改良されてきたよ。たとえば、「密閉型鉛蓄電池」というものがあって、これは内部のガスを外に逃がさない仕組みになっているんだ。これによってメンテナンスの手間が少なくなるし、効率も向上しているんだ。こうした改良によって、鉛蓄電池はますます便利になっているんだよ。
例題&解答
【例題1】
鉛蓄電池で、充電時に負極・正極で起こる反応式を示しなさい。
負極:PbSO₄ + 2e⁻ → Pb + SO₄²⁻
正極:PbSO₄ + 2H₂O → PbO₂ + SO₄²⁻ + 4H⁺ + 2e⁻
【例題2】
鉛蓄電池が再び充電可能である理由を説明しなさい。
放電時の反応を逆に進めることで、鉛と酸化鉛を再び生成し、電池がエネルギーを蓄えることができるため、再び充電可能である。











