ページのまとめ(所要時間:7分)
学習のポイント
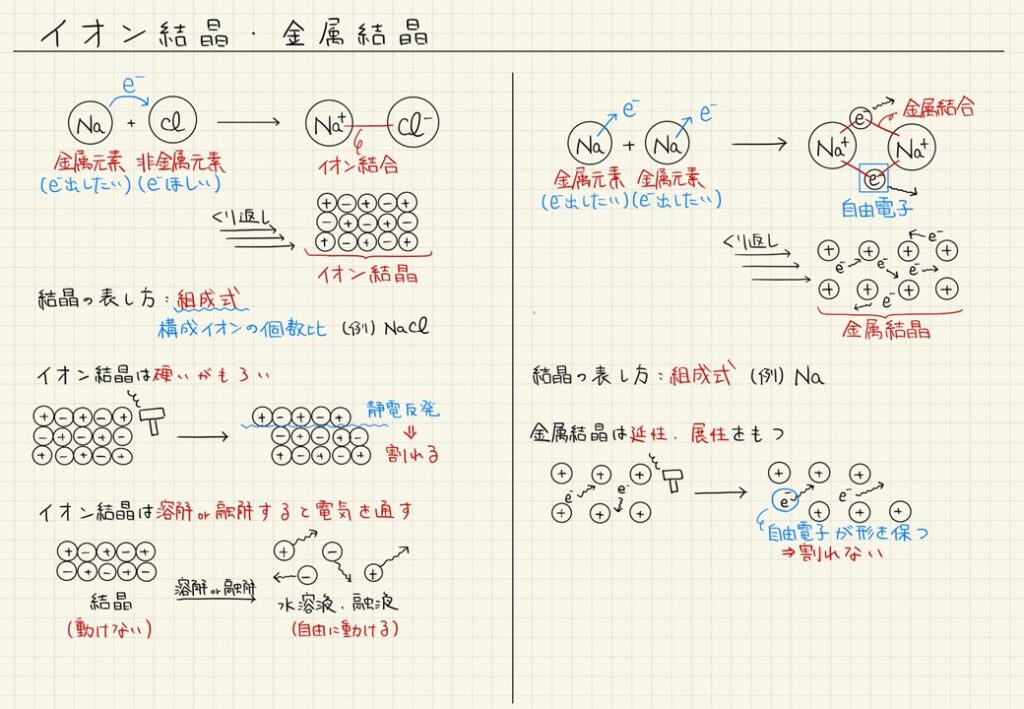
- イオン結合は、陽イオンと陰イオンが静電気的に引き合って結びつく化学結合。
- 代表的な例は**塩化ナトリウム(NaCl)で、ナトリウムイオン(Na⁺)と塩化物イオン(Cl⁻)が結びついている。
- イオン結晶は、規則正しく並んだイオンで構成された結晶で、強い結晶構造を持ち、融点が高い。
- イオン結晶は水に溶けると電気を通す性質を持つ。
- 他の例としては酸化マグネシウム(MgO)や硫酸カルシウム(CaSO₄)がある。
まとめノート
~先生と生徒の会話~
 先生
先生今日は「イオン結合」と「イオン結晶」について説明しようか。聞いたことある?



うーん、名前は聞いたことがあるけど、どういう仕組みかはよくわからないです…。



そうだよね、まずイオン結合っていうのは、異なる電荷を持つイオン同士が静電気的な力で引き合うことで結びつく現象なんだ。たとえば、ナトリウム(Na)は電子を1つ失ってナトリウムイオン(Na⁺)になり、塩素(Cl)は電子を1つ受け取って塩化物イオン(Cl⁻)になる。これらが引き合って塩化ナトリウム(NaCl)という物質ができるんだ。この図を見てみよう。
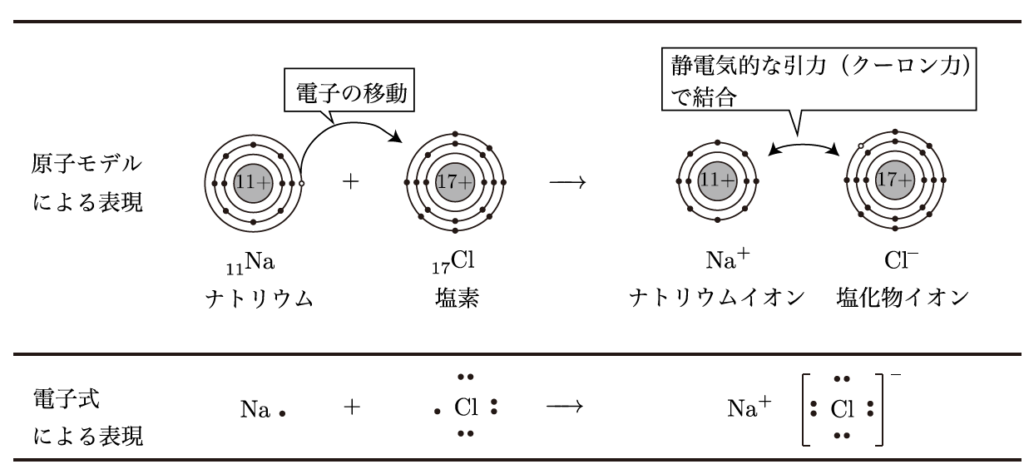




ナトリウムと塩素が電子をやり取りして結びつくんですね!それで塩ができるんですか?



その通り。ナトリウムは電子を放出して陽イオンになり、塩素はその電子を受け取って陰イオンになる。このようにして陽イオンと陰イオンが引き合ってできる結合が、イオン結合なんだ。この結合が形成されることで、各元素は希ガスと同じ安定した電子配置を手に入れるんだよ。



じゃあ、イオン結晶って何ですか?



いい質問だね。イオン結晶は、規則正しく並んだイオンの集まりで構成された固体のことなんだ。たとえば、塩化ナトリウムは、ナトリウムイオンと塩化物イオンが交互に規則正しく並んで、結晶格子を作っているんだ。だから、塩の結晶は小さくても硬くて、きれいな形をしているんだよ。



そういえば、塩は結晶の形がきれいですよね。それがイオン結晶なんですね!



そうなんだ。この結晶構造はとても強くて、融点が高いのが特徴だよ。塩化ナトリウムの融点は約800℃もあるんだ。これは、イオン同士が非常に強く引き合っているからなんだ。それに、固体の状態では電気を通さないけど、水に溶けるとイオンが自由に動けるようになるので、電気を通すことができるんだよ。



塩を水に溶かすと電気を通すって、すごいですね!他にはどんなイオン結晶があるんですか?



たとえば、酸化マグネシウム(MgO)や硫酸カルシウム(CaSO₄)もイオン結晶の一例だね。これらも同じように陽イオンと陰イオンが結びついて、強固な結晶構造を作っているんだ。
例題&解答
【例題1】
次の化学物質のうち、イオン結合で結ばれているものはどれですか?
・塩化ナトリウム(NaCl)
・水(H₂O)
・酸素(O₂)
【解答】
塩化ナトリウム(NaCl)
【例題2】
イオン結晶が融点が高い理由を簡単に説明しなさい。
【解答】
イオン結晶では、陽イオンと陰イオンが強く引き合って結晶格子を形成しているため、融点が非常に高くなる。













