このページのまとめ
学習のポイント
- イオン結晶の結晶格子には、NaCl型・CsCl型・ZnS型などが存在する。
- NaCl型の単位格子中に正味4個ずつのイオンが存在し、限界イオン半径比は√2-1から√2+1までである。
- CsCl型の単位格子中に正味1個ずつのイオンが存在し、限界イオン半径比は√3-1から(√3+1)/2までである。
- ZnS型の単位格子中に正味4個ずつのイオンが存在し、限界イオン半径比は(√6-2)/2から√6+2までである。
まとめノート

このページでは、イオン結晶の単位格子について解説していきます。イオン結晶の単位格子は様々なものがありますが、高校化学の範囲では塩化ナトリウム型、塩化セシウム型、閃亜鉛鉱型の3つを主に扱います。それぞれの単位格子について、正味の数・配位数・限界イオン半径比が重要となりますから、それぞれ確認していきましょう。
イオン結晶の結晶格子
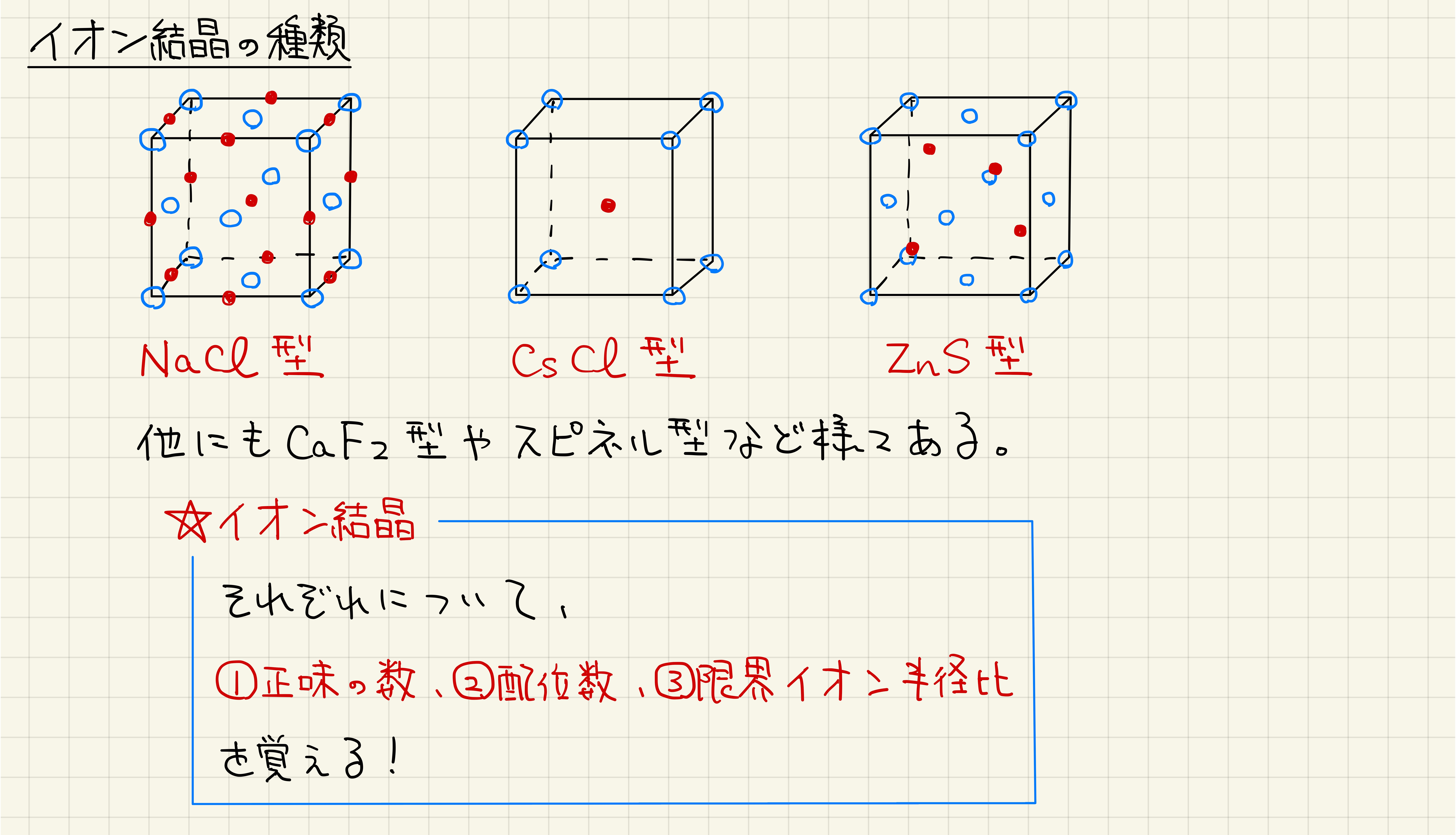
先述したように、イオン結晶の単位格子には様々な種類が存在しています(金属結晶では面心立方格子・体心立方格子・六方最密構造の3種類だけでした)。高校化学の範囲では塩化ナトリウム型、塩化セシウム型、閃亜鉛鉱型を主に扱うので、これらについて確認していきましょう。それぞれの結晶について、正味の数・配位数・限界イオン半径比を求められるようにすることが目標です。
NaCl型結晶
正味の数・配位数

まず初めに、塩化ナトリウム型について学習していきます。図に示している結晶では、陰イオンが面心立方格子の位置に配置し、陽イオンがその間にはいる形で結晶が構成されています。面心立方格子の正味の数は4個でしたから、同様に陰イオンの正味の数も4個となります。また、陽イオンも正味の数は4個となっており、陽イオンと陰イオンの個数が同じことから、組成比が1:1とわかります。
次に配位数に関して見ていくと、陽イオンに近接している陰イオンの数は6個となります。同様に、陰イオンに近接している陽イオンの数も6個です。塩化ナトリウム型結晶においては陽イオンと陰イオンの価数が等しいことから、必ず配位数は等しくなります。
限界イオン半径比

塩化ナトリウム型結晶の限界イオン半径比について見ていきましょう。限界イオン半径比とは、その結晶構造を取ることができる最大または最小の陽イオンと陰イオンの比です。
限界イオン半径比を考える際には、断面を取ることが重要です。塩化ナトリウム型結晶の面で見ると、格子定数aと陰イオンおよび陽イオンの関係式が得られます。次に陰イオンを限界まで大きくすることを考えると(陰イオン同士が接する状態が限界)、格子定数と陰イオン半径の関係式が得られます。ここで得られた2式を連立して解くと、√2ー1という陽イオンと陰イオンの比が得られます。これが陰イオンを大きくした際の限界イオン半径比です。
陽イオンを大きくした場合は比の逆数を取ればよく、√2+1となります。すなわち、陽イオンと陰イオンの半径比が√2-1から√2+1の間にある組み合わせであれば、塩化ナトリウム型結晶をとることができるということになります。
CsCl型結晶
正味の数・配位数

次に、塩化セシウム型結晶について学習していきます。図に示した結晶では、陰イオンが単位格子の頂点に位置し、陽イオンが単位格子の中心に位置しています。したがって、正味の数は両者とも1個となっています。先程の塩化ナトリウム型結晶と同様に、個数比が同じことから組成比も1:1であることが分かります。
配位数について確認していきましょう。陽イオンに近接している陰イオンの数は8個です。同様に陰イオンに近接している陽イオンも8個となっています。これは、塩化セシウム型のイオン結晶も陽イオンと陰イオンの価数比が1:1であることを表しています。
限界イオン半径比
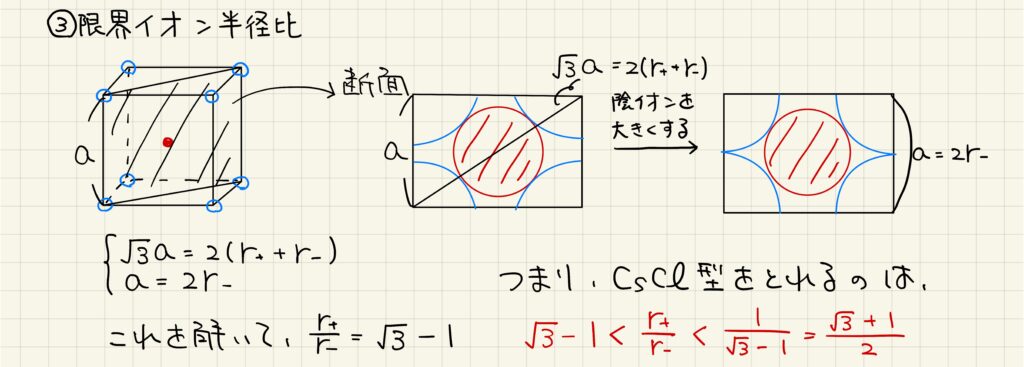
塩化ナトリウム型と同様に断面を取って限界イオン半径比を考えていきましょう。体対角の断面を見ると格子定数と陽イオン半径、陰イオン半径の関係式が得られます。さらに陰イオンを大きくしていくことで格子定数と陰イオン半径の関係式が得られます。これらを連立して解くことで限界半径比が得られます。
塩化セシウム型を取ることができるのは、陽イオンと陰イオンの半径比が√3ー1から(√3+1)/2の間にある組み合わせとなります。尚、塩化セシウム型結晶では配位数が8個と塩化ナトリウム型の6個よりも多いので、より安定な構造と言えます。限界イオン半径比の条件で両方の結晶構造を取ることができる場合には、塩化セシウム型を優先して取ることが知られています。
ZnS型結晶
正味の数・配位数
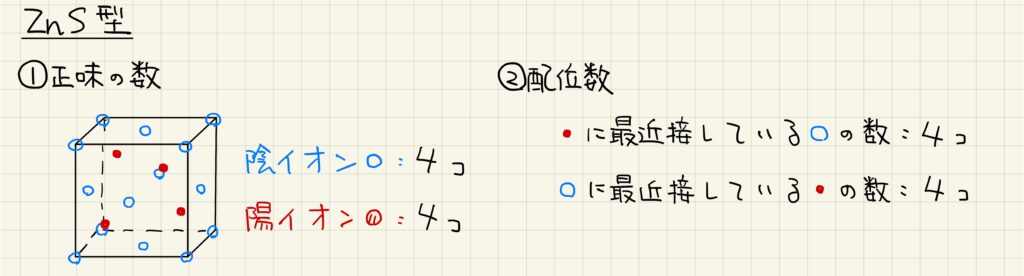
最後に、閃亜鉛鉱型の結晶について見ていきましょう。閃亜鉛鉱型結晶では、陰イオンが面心立方格子と同じ配置をしています。したがって、陰イオンの正味の数は4個です。陽イオンは、陰イオンがつくる正四面体隙間のうち半分に存在しています。したがって、正味の数は4個です。閃亜鉛鉱も組成比が1:1なので、正味の数が同数となることも説明がつきます。
配位数に関しては、陽イオン・陰イオンともに4個となっています。価数比が1:1なので、それぞれの配位数も等しくなります。
限界イオン半径比
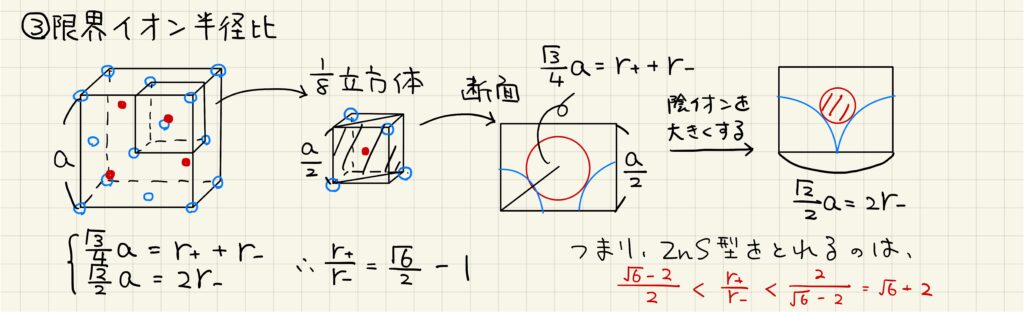
閃亜鉛鉱型の限界イオン半径比を求めていきましょう。単位格子では考えにくいので、1/8立方体をとって見るとわかりやすいです。条件式を2本立て、それらを連立することで限界イオン半径比を求めます。
閃亜鉛鉱型では、陽イオンと陰イオンの半径比が(√6ー2)/2から√6+2の間にある場合に取ることができます。閃亜鉛鉱型の結晶は2価のイオンで構成されるイオン結晶の場合につくられることが多いです。













