このページのまとめ
学習のポイント
- 物質は混合物と純物質に分けられ、純物質はさらに単体と化合物に分けられる。
- 同素体とは、同じ元素から構成されるが、互いに性質が異なる単体のことを指す。
- 炭素、硫黄、酸素、リンで同素体が存在する。
まとめノート

このページでは,物質の分類や同素体について解説していきます。また,元素・原子・単体は同じ言葉で語られることがあるので,違いを確認しておく必要があります。さらに,同素体は同じ元素からなるが性質が異なる単体です。炭素・硫黄・酸素・リンが同素体を持つことが知られているので,それぞれの性質について確認していきましょう。
物質の分類
純物質と混合物
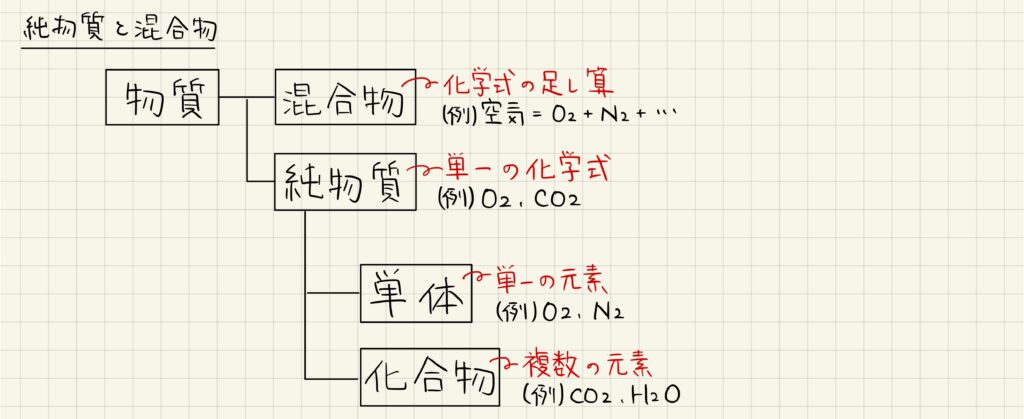
世の中に存在する物質は,全て純物質と混合物に分類することができます。純物質とは,単一の化学式で表すことができ,一切の不純物が混ざっていない状態です。対して混合物とは,様々な物質が混ざり合って存在している状態です。例えば,大気は酸素と窒素とその他多くの気体の混合物として知られています。
純物質のうち,単一の元素からなるものを単体,複数の元素からなるものを化合物と呼びます。例えば,酸素や窒素は単体,二酸化炭素や水は化合物に分類されます。
元素・原子・単体

元素・原子・単体は同じ言葉で説明されることがあり,文脈から意味を捉えなければなりません。例えば,上の3つの文章を見てみましょう。⑴の例では,O2としての酸素分子のことが述べられています。したがって,これは単体の意味です。⑵の例では,酸素という元素が同位体の区別なく地殻中に含まれていることを示しています。つまり,これは元素の意です。⑶の例では,酸素原子の結合についての文章ですから,これは原子の意味となります。同じ「酸素」という言葉ですが,文脈によって意味が異なりますから注意しておきましょう。
同素体
同素体の定義

同素体とは,「同じ元素から構成されるが,互いに性質が異なる単体」のことを指します。例えば,同じ炭素だけから構成される黒鉛とダイヤモンドなどが挙げられます。
似た言葉に,同位体というものがあります。同位体とは,「原子番号は同じだが,中性子数が異なり質量数が違う原子」のことです。同素体は単体であるのに対して同位体は原子なので,違いをよく理解しておきましょう。
炭素の同素体
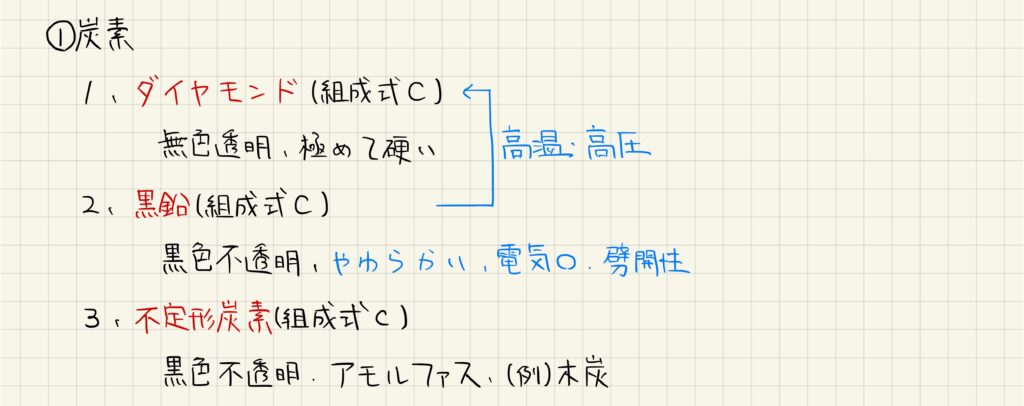
炭素は,非常に多くの同素体を持ちます。ダイヤモンドは炭素だけからなる共有結合結晶で,組成式Cで表されます。無色透明で,自然界で最も硬い物質として知られています。
黒鉛は,ダイヤモンドと同様に共有結合結晶で,組成式Cで表されます。ダイヤモンドと性質が異なり,黒色不透明,柔らかく,電気を通し,劈開性があることが知られています。また,黒鉛を高温・高圧下におくことでダイヤモンドを得ることができます。
不定形炭素は,炭素原子が不規則に配列してアモルファスの状態になったものです。組成式Cで表され,黒色不透明です。木炭などには不定形炭素が多く含まれています。

フラーレンは,炭素原子60個がサッカーボール状の分子を形成してできる物質です。分子式C60で表されます。フラーレンを用いた超電導性の研究が行われています。
カーボンナノチューブは,炭素原子が筒状に結合してできる高分子です。引っ張り強度が強く,革新的な用途での利用が期待されています。
硫黄の同素体

硫黄は,3種類の同素体を持ち,全て黄色の物質です。斜方硫黄および単斜硫黄は同じ王冠状分子を形成しており,分子式S8で表されます。ただし,斜方硫黄は常温で安定な構造を作るのに対して,単斜硫黄は比較的高温で安定な構造をとります。
ゴム状硫黄は硫黄原子が無数に結合してできる高分子です。組成式Sで表されます。ゴム状硫黄の名の通り,弾性があることで知られています。
酸素の同素体
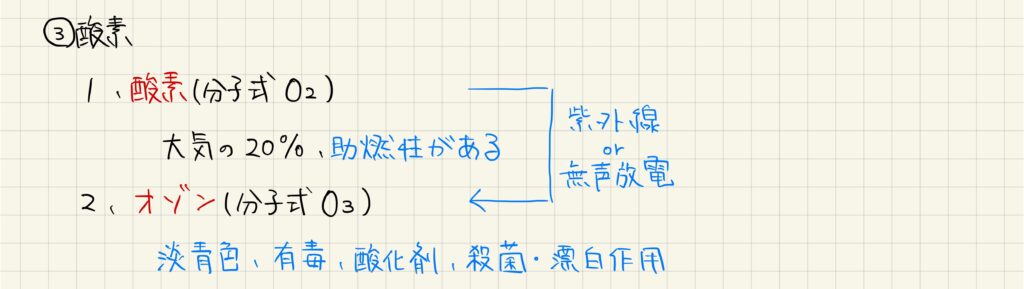
酸素には,2種類の同素体があります。分子式O2で表される酸素分子は,大気の20%を占める気体で,助燃性があります。この酸素分子に紫外線を当てたり無声放電をすることで,分子式O3で表されるオゾンが生じます。オゾンは淡青色の有毒気体で,酸化剤として働き,殺菌・漂白作用があります。
リンの同素体

リンは2種類の同素体をもちます。分子式P4で表される黄リンは有毒で,自然発火するために水中で保存します。一方,組成式Pで表される赤リンは無毒です。赤リンは発火点が低いことから,マッチ箱の側面に塗られています。













