このページのまとめ
学習のポイント
- 元素周期表は、原子番号の順に並んでいて、横の列(周期)と縦の列(族)に分けられる。
- 1族のアルカリ金属や2族のアルカリ土類金属は反応性が高い。17族のハロゲン元素も反応性が強く、18族の希ガス元素は非常に安定している。
- 周期表には、おおよそ左側に金属元素、右側に非金属元素が配置されている。
- 遷移元素は、周期表の中央に位置し、一般的な金属の性質と特異な化学反応を持つ。
まとめノート
~先生と生徒の会話~
 先生
先生今日は「元素周期表」について詳しく話してみようか。教科書や実験室で見かける周期表には、実はたくさんの情報が詰まっているんだよ。



確かに、記号や数字がいっぱいありますよね。でも、どうやって読むのかはよくわかりません。



そうだよね。でも、周期表を理解すると、化学の世界が一気に広がるんだ。周期表には元素が原子番号の順に並んでいるだけでなく、周期と族によって、元素の性質や反応性を予測できるんだ。



周期と族ってなんですか?



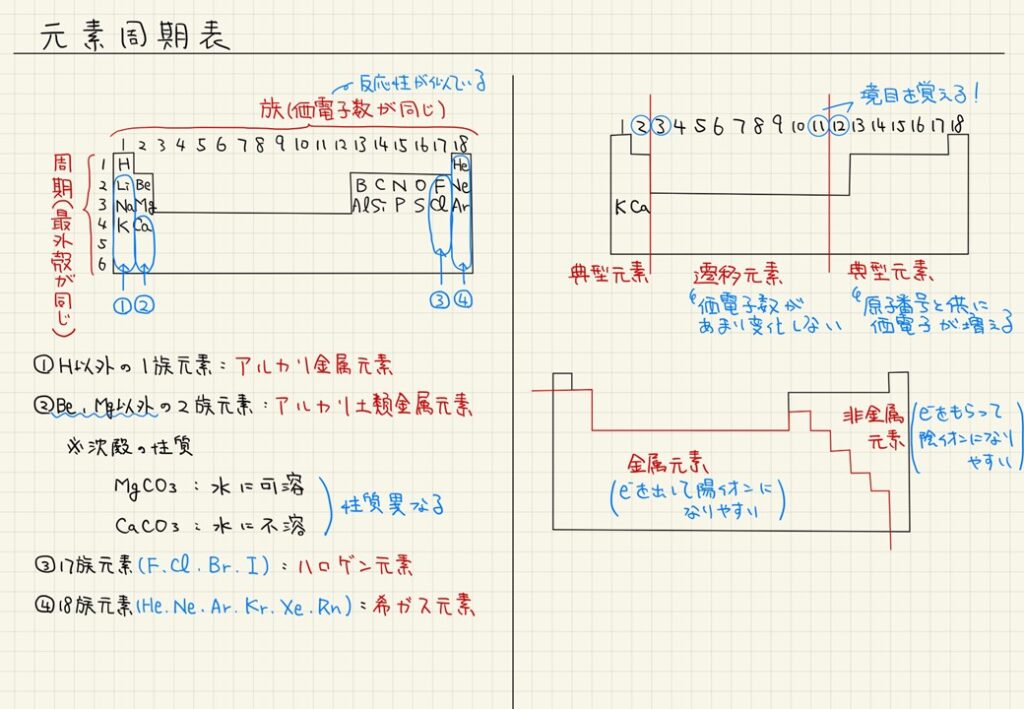
周期は、周期表の横の列で、原子の電子配置に対応している。周期が進むにつれて、元素の性質が少しずつ変わっていくんだ。族は縦の列で、同じ族に属する元素は、価電子の数が同じだから、化学反応の性質が似ているんだよ。この図を見てみよう。
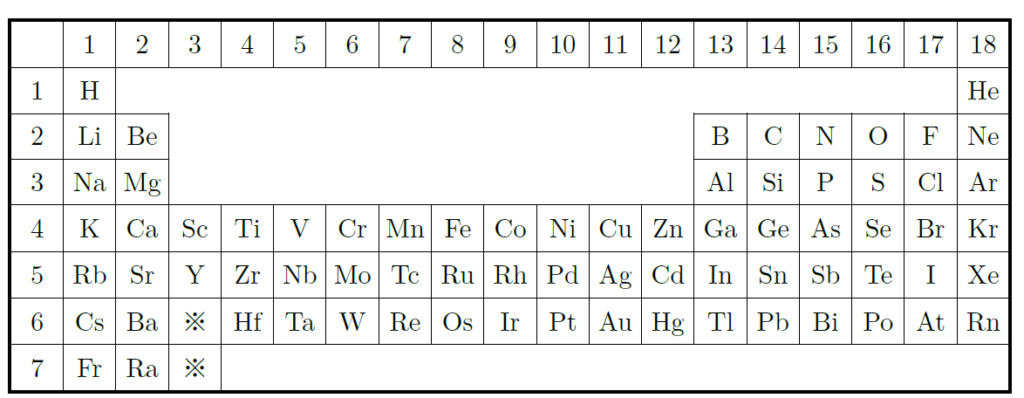




なるほど、周期と族に意味があるんですね。



その通り。例えば、1族のアルカリ金属は価電子が1個で、非常に反応性が高い。ナトリウムやカリウムは、水と反応すると激しく爆発することがあるよ。次に、2族のアルカリ土類金属は、2個の価電子を持っていて、反応性は少し落ちるけど、やはり反応しやすいんだ。マグネシウムやカルシウムがその代表だね。



アルカリ金属は反応が強いんですね。じゃあ、他の族はどうなんですか?



他にも、17族のハロゲン元素も非常に反応性が高いんだ。例えば、フッ素や塩素は、他の元素と結びついて塩を作るのが得意だよ。反対に、18族の希ガス元素は、最外殻の電子が満たされているから、ほとんど反応しないんだ。ヘリウムやネオンがその例だね。



なるほど、族ごとに性質が違うんですね。それに、金属と非金属もあるんですよね?



そうだね。周期表の左側には金属元素が多く、右側には非金属元素が多い。金属は電気や熱をよく通す性質があり、光沢があるものが多いんだ。一方、非金属は電気を通しにくく、脆いことが多いね。下の図では灰色に塗られた元素が非金属元素だよ。
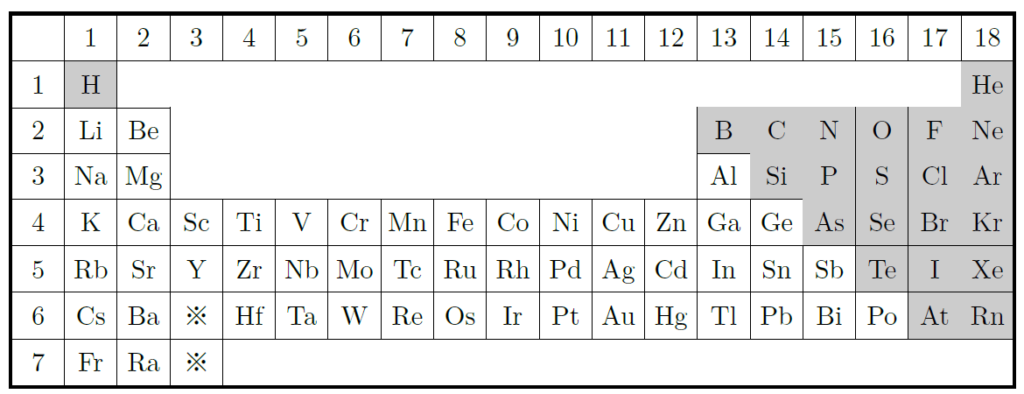




金属と非金属で違うんですね。



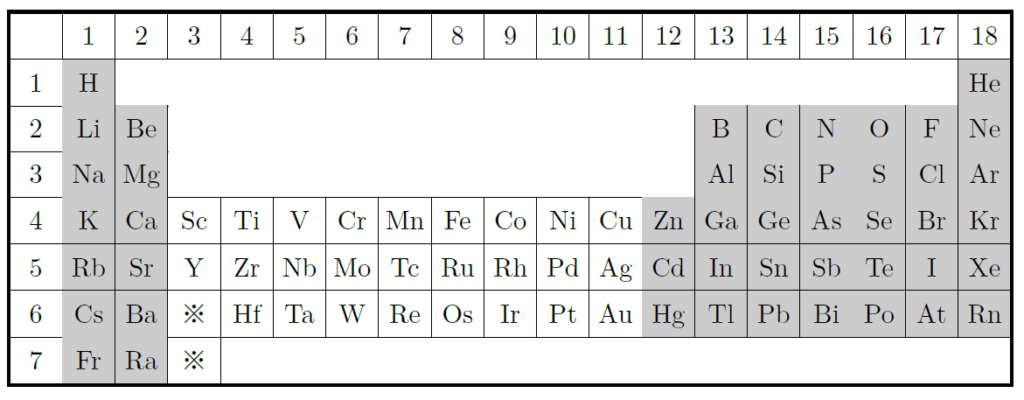
そして、周期表の中央には遷移元素と呼ばれる金属が並んでいるんだ。これらの元素は、典型的な金属の性質を持ちながらも、化学反応では少し違った動きをすることがあるんだ。だから、「典型元素」と「遷移元素」に分けられることもあるんだよ。下の図では、灰色に塗られた元素が典型元素に当たるね。

例題&解答
【例題1】
次のうち、17族に属する元素はどれですか?
・フッ素(F)、リチウム(Li)、カルシウム(Ca)
【解答】
フッ素(F)
【例題2】
遷移元素と典型元素の違いを説明しなさい。
【解答】
遷移元素は、周期表の中央に位置し、金属の性質を持ちながら特異な化学反応を示す。典型元素は、遷移元素以外の元素で、規則的な化学性質を持つ。













