このページのまとめ
学習のポイント
- 原子は陽子、中性子、電子で構成されており、中心の原子核のまわりを電子がまわっている。
- 陽子数を原子番号と呼び、陽子数と中性子数の和を質量数と呼ぶ。
- 原子番号は同じだが、質量数が異なる原子を同位体という。
まとめノート
このページでは,原子の構造,同位体,電子配置について解説します。理論化学を学ぶ上で,これらの内容は基本となる部分です。私たちの身の回りに存在している全ての物質は原子からできており,その構造を理解することで今後の化学反応を学ぶための基礎が出来上がります。化学を学ぶための第一歩として,原子の構造を学んでいきましょう。
【原子】原子は陽子,中性子,電子から構成される
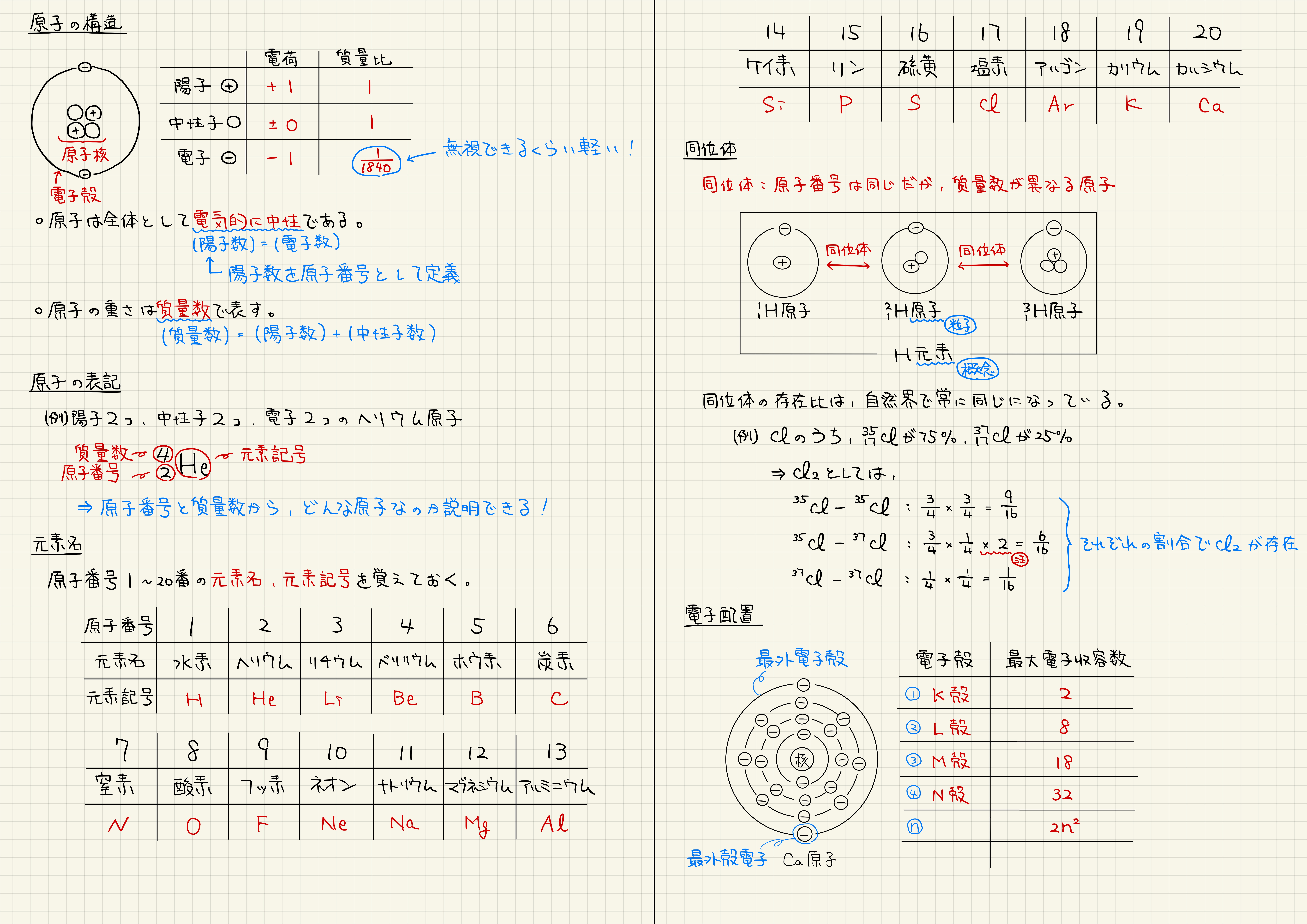
原子の構造

原子とは,私たちの体や大気中の酸素など,あらゆる物質を構成している小さな単位です。原子の中心部には原子核があり,その周りを電子殻に沿って電子が回っています。原子核は陽子と中性子から構成されており,その質量はほぼ同じですが,陽子は正の電荷を持つのに対し,中性子は電荷を持ちません。電子は非常に質量が小さく,負の電荷を帯びています。
原子は全体として電気的に中性であるという性質があり,正の電荷と負の電荷がつり合っています。つまり,陽子数と電子数が同じになっています。陽子数は原子番号という数字で定義し,元素を区別するためによく用いられています。また,原子の質量は質量数で表されます。電子の質量が十分小さいために,質量数は陽子数と中性子数の和で計算されます。
原子の表記

原子は,元素記号の左上に質量数,左下に原子番号を添えて表記します。原子番号は陽子数を表すので,原子番号から陽子の数が分かります。さらに,原子は全体で電気的に中性であるという条件から陽子数と電子数が等しいので,電子の数も分かります。最後に,質量数は陽子数と中性子数の和なので,質量数から原子番号を引けば中性子数が分かります。このように,質量数と原子番号が分かれば,原子中の陽子・中性子・電子の数が判明し,原子を表すことができます。
【元素名】原子番号20番までは必ず覚える
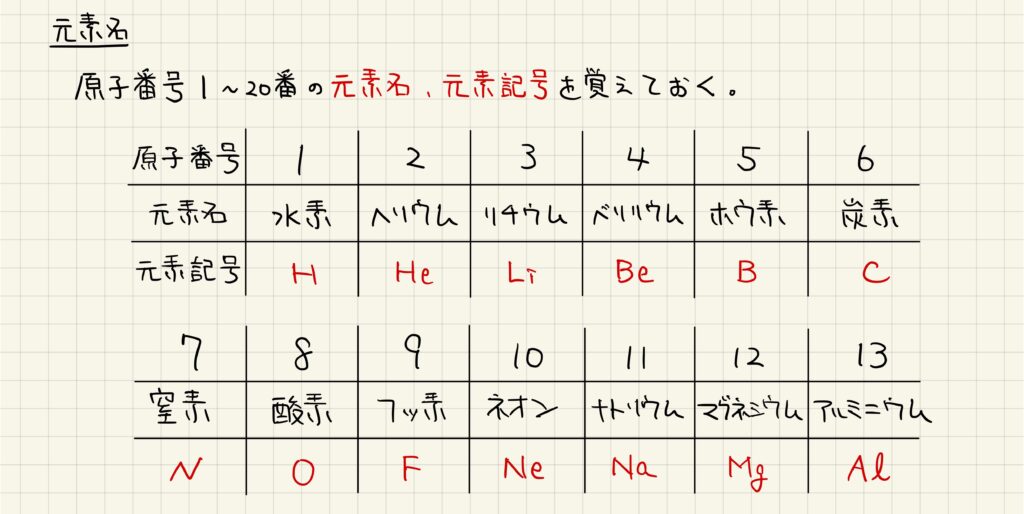
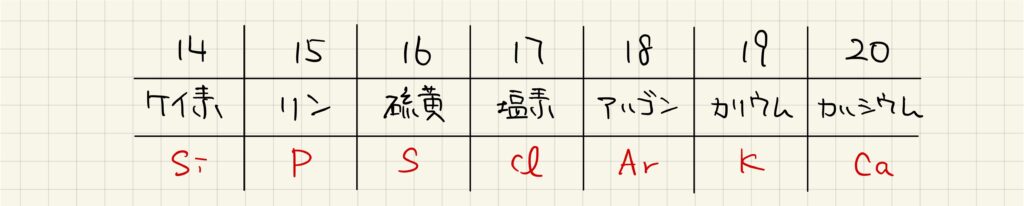
まずは,原子番号20番までの元素について,原子番号・元素名・元素記号を覚えておきましょう。例えば,二酸化炭素はCO2で表されますが,これは炭素原子1つと酸素原子2つから構成されていることが分かります。加えて,原子番号20番以降の元素についても教材に出てきたものから順に覚えていくようにしましょう。
【同位体】同じ元素でも中性子数が異なる原子がある
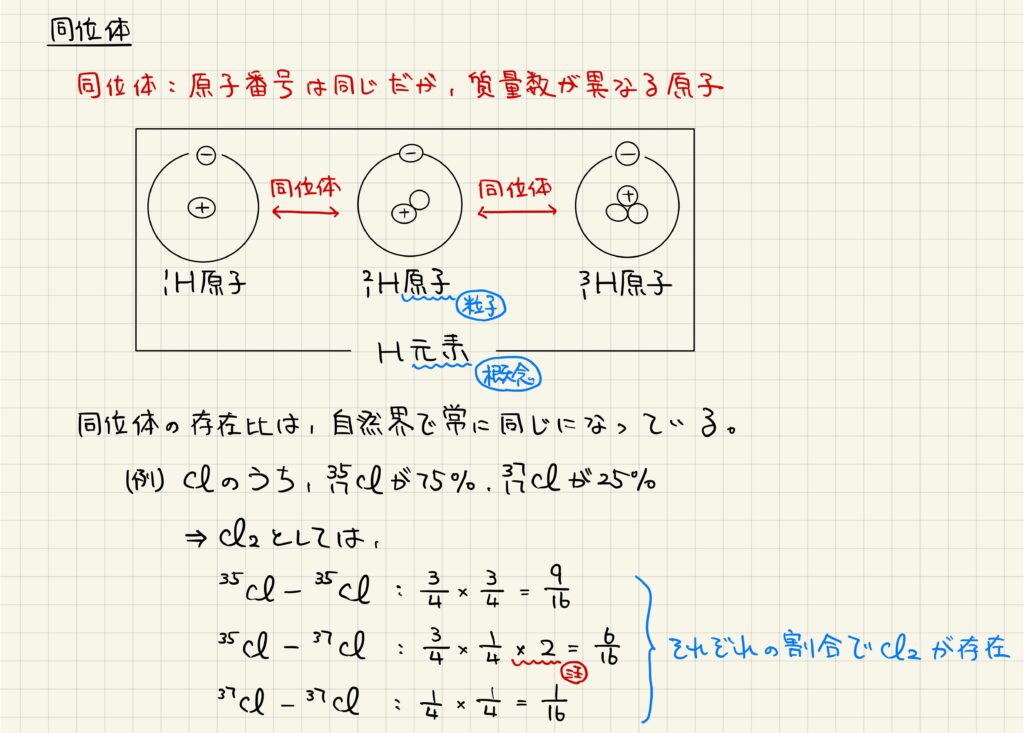
原子番号は同じだが,質量数が異なる原子のことを同位体と呼びます。例えば,水素には質量数が2の重水素や質量数が3の三重水素が同位体として存在します。これらはいずれも原子番号が1の水素原子であり,全てをまとめて水素元素と呼んでいます。
同位体は自然界のどこでも同じ割合で存在しており,原子どうしが結合した分子に関してもその存在比を求めることができます。例えば,質量数35の塩素原子と質量数37の塩素原子が3:1で存在しているとすると,3パターンの塩素分子がそれぞれの割合で存在していることになります。数学的な組み合わせとして計算できるので,計算方法を覚えておきましょう。
【電子配置】電子は電子殻に分かれて周回している
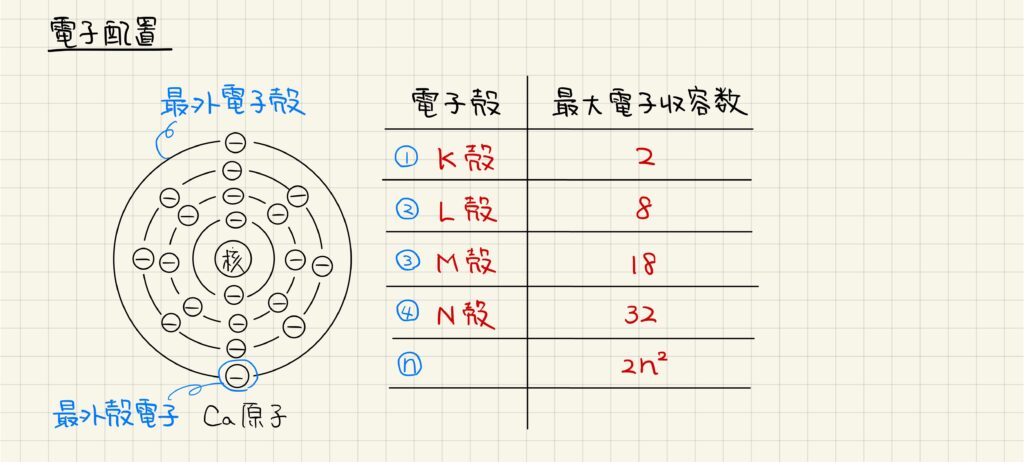
電子はそれぞれの電子殻に分かれて,原子核の周りを回っています。内側から順にK殻,L殻,M殻,N殻・・・と続いていきます。最も外側にある電子を最外殻電子と呼び,最外殻電子が属する電子殻を最外電子殻(最外殻)と呼びます。
それぞれの電子殻には収容することができる電子の数が決まっており,内側からn番目の殻には2n2個の電子が収容可能です。また,基本的には内側の電子殻から順に電子が埋まっていきます。ただし,Ca原子の電子配置を見ると,M殻がまだ満タンではないのにN殻に電子が入っています。これはオクテット則といい,電子殻に8個の電子が収容されている状態で少し安定な構造となるのです。












