このページのまとめ
学習のポイント
- 金属イオンが複数混合している水溶液から、沈殿を用いて1つずつ分離していくことができる。
- 塩化物イオンは銀イオン・鉛イオン・水銀イオンとのみ沈殿をつくる。
- 硫化物イオンはpHによって沈殿をつくる金属イオンが異なる。
- 水酸化物イオンはアルカリ金属・アルカリ土類金属以外の金属イオンと沈殿をつくる。
- 炭酸イオンはアルカリ金属以外の金属イオンと沈殿をつくる。
まとめノート
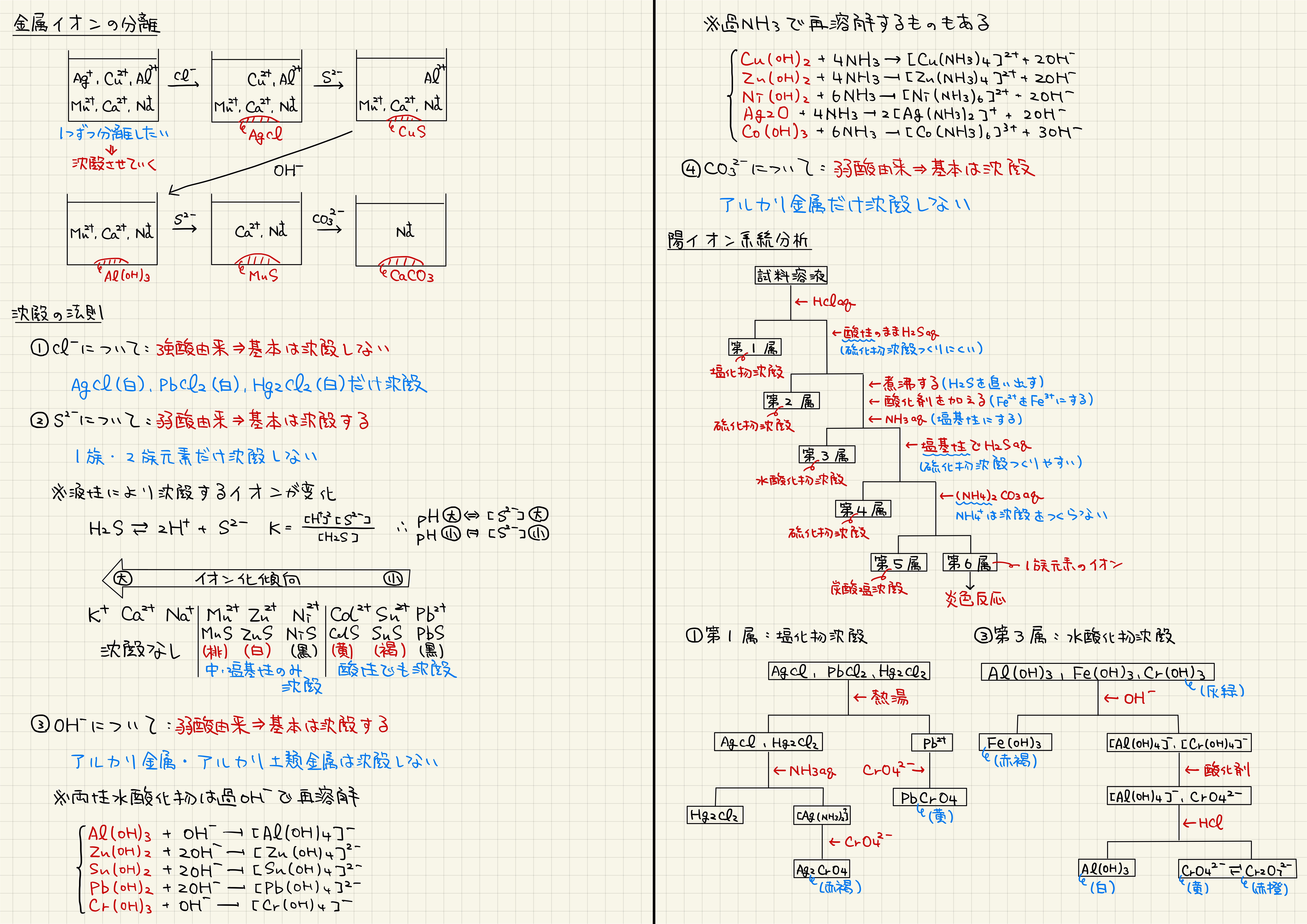
このページでは,金属イオンの分離について解説していきます。金属イオンがいくつか混合している溶液から,一つずつを沈殿させて分離する操作があります。この操作を系統分析と呼び,実験手順は明確に決まっています。金属イオンがどのように沈殿し,分離されていくのか,学んでいきましょう。
金属イオンの分離
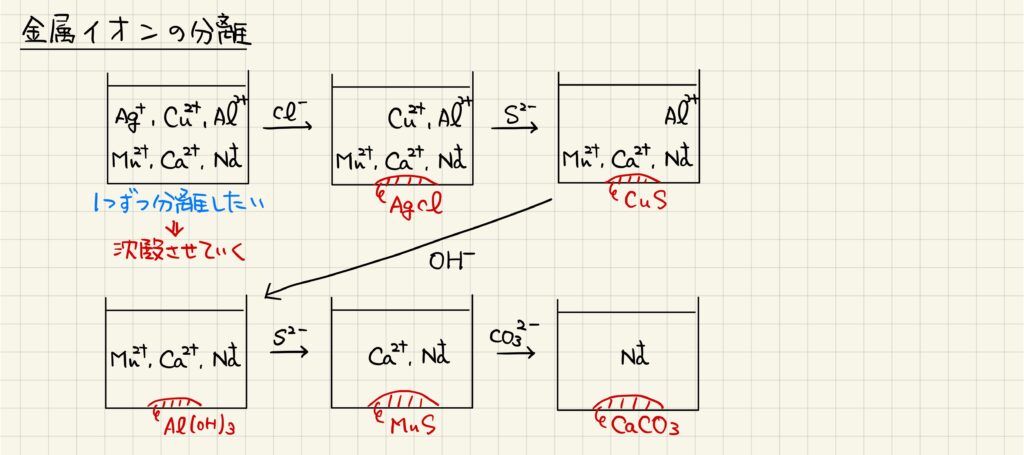
溶液中に複数種類の金属イオンが混合しているとき,一つずつを沈殿させることで分離することができます。例えば,銀イオン,銅イオン,アルミニウムイオン,マンガンイオン,カルシウムイオン,ナトリウムイオンが混合している状況を考えてみましょう。まず塩化物イオンを加えることで,塩化銀のみが沈殿します。次に酸性条件で硫化物イオンを加えると,硫化銅のみが沈殿します。そこへ塩基を加えて塩基性にすると,水酸化アルミニウムが沈殿します。さらに塩基性条件下で硫化物イオンを加えると硫化マンガンが沈殿し,最後に炭酸イオンを加えることで炭酸カルシウムが沈殿します。このように,それぞれのイオンを順に沈殿させることで,金属イオンを分離することができます。
沈殿の法則
塩化物沈殿について

では次に,どのような組み合わせで沈殿が形成されるのか見ていきましょう。塩化物イオンは強酸である塩酸由来のイオンなので,安定なイオンです。したがって,塩化物イオンは基本的には沈殿しないですが,例外的に銀イオン,水銀イオン,鉛イオンと沈殿を形成します。
硫化物沈殿について

硫化物イオンは弱酸である硫化水素由来のイオンなので基本的に不安定で,沈殿を形成しやすいです。ただし,硫化物イオンは1族元素や2族元素とは沈殿を形成しません。硫化物沈殿は溶液の液性によって沈殿形成の有無が変化します。pHが大きい(塩基性)の方が硫化物イオンが多く存在し,硫化物沈殿を作りやすくなっています。そのため,イオン化傾向が大きい金属イオンは塩基性条件下でしか硫化物沈殿を作らず,対してイオン化傾向が小さい金属イオンは酸性条件でも(もちろん塩基性条件でも)硫化物沈殿を作ります。
水酸化物沈殿について

水酸化物イオンは水由来のイオンと考えることができるので,基本的に不安定であり,沈殿しやすいです。水酸化物イオンは、例外的にアルカリ金属・アルカリ土類金属とは沈殿を形成しません。
両性元素は過剰の塩基を加えることで,水酸化物沈殿が再溶解することが知られています。例えばアルミニウムの場合は,水酸化アルミニウムからテトラヒドロキシドアルミン酸イオンが形成されます。

その他にも,過剰のアンモニアと反応して再溶解するものがあります。具体的には,銅,亜鉛,ニッケル,銀,コバルトです。例えば銅の場合では,水酸化銅からテトラアンミン銅(Ⅱ)イオンが形成されます。
炭酸塩について

炭酸イオンは弱酸である二酸化炭素由来の不安定イオンであり,基本的には沈殿を形成します。ただし,炭酸イオンはアルカリ金属のイオンとだけは沈殿を形成しません。
陽イオン系統分析
系統分析の実験操作
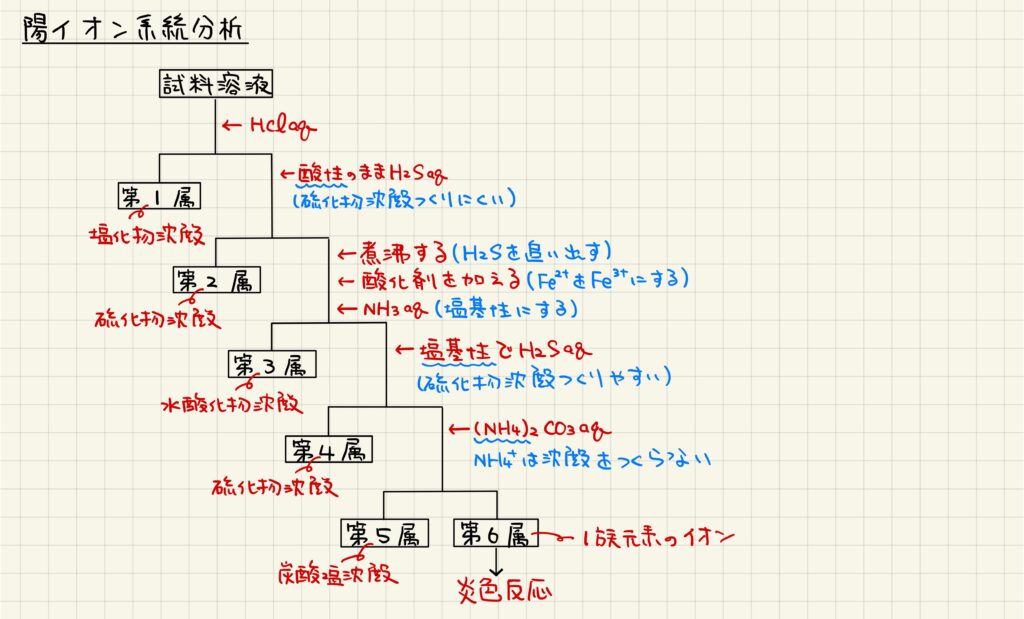
これまでの沈殿の法則を踏まえて,金属イオンを分離するために特定の操作手順が存在します。これが系統分析です。系統分析では,①塩酸を加える,②酸性条件下で硫化水素を加える,③煮沸した後酸化剤を加え,塩基を添加して塩基性にする,④塩基性条件下で硫化水素を加える,⑤炭酸アンモニウムを加える,⑥炎色反応を行う,という順に操作を行います。それぞれの操作によって特定の沈殿が形成され,金属イオンを分離することができます。
③において煮沸する,酸化剤を加える理由が頻繁に問われます。煮沸は,直前に加えて硫化水素を取り除くためです。ここで硫化水素を取り除いておかないと,水酸化物沈殿と硫化物沈殿が混合されてしまいます。また,酸化剤を加えるのは,硫化水素によって還元されてしまった鉄イオンを鉄(Ⅲ)イオンに戻すためです。鉄の水酸化物は水酸化鉄(Ⅲ)の方が沈殿しやすいため,このような操作を行います。
属内の分離
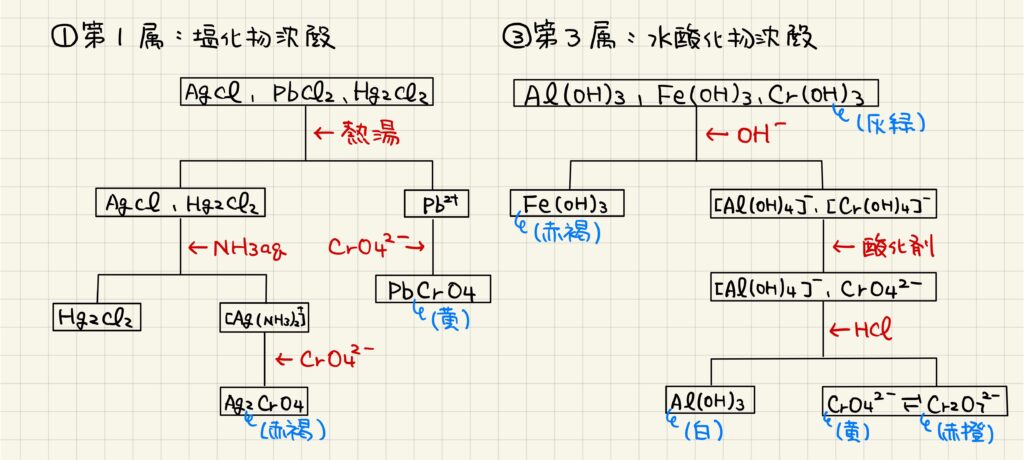
系統分析によってそれぞれの属に金属イオンを分離できますが,同じ属内に複数のイオンが含まれる場合があります。ここでは,第1属と第3属の分類を見ていきましょう。
第1属は塩化物沈殿のカテゴリーで,塩化銀,塩化鉛,塩化水銀などが含まれます。まずはこれらを熱湯に加えると,塩化鉛のみが溶解して分離することができます。次に沈殿に対してアンモニアを加えると,塩化銀は錯イオンを形成して再溶解するので完全に分離することが可能です。
第3属は水酸化物沈殿のカテゴリーで,水酸化アルミニウム,水酸化鉄(Ⅲ),水酸化クロムなどが含まれます。まずは過剰の塩基を加えることで,両性水酸化物である水酸化アルミニウムと水酸化クロムのみが再溶解します。次に酸化剤を加えるとクロムの錯イオンがクロム酸イオンに変化し,そこへ酸を加えると水酸化アルミニウムのみが沈殿します。以上で,全ての沈殿を分離することができました。