このページのまとめ
- 錯イオンは、金属イオンが配位子に囲まれてできる複合イオンです。
- 錯イオンの構造は、配位数によって決まり、典型的な錯イオンにはテトラアンミン銅(II)イオン [Cu(NH₃)₄]²⁺やヘキサアクア鉄(III)イオン [Fe(H₂O)₆]³⁺があります。
- 錯イオンは、錯滴定や触媒反応など、化学反応において重要な役割を果たしています。
~先生と生徒の会話~
 生徒
生徒錯イオンって、聞いたことがあるんですけど、どういうものなんですか?



錯イオン(さくイオン)というのは、金属イオンが配位子と呼ばれる分子やイオンに囲まれてできた複合イオンのことなんだ。金属イオンが中心にあって、その周りに配位子が結びつくことで安定した構造を形成するんだよ。この配位子は金属イオンに対して「電子対」を提供して結合するんだ。



例えば、アンモニア(NH₃)や水(H₂O)がよく配位子として使われるんだ。錯イオンは、水溶液中や結晶の中でよく見られる構造だよ。
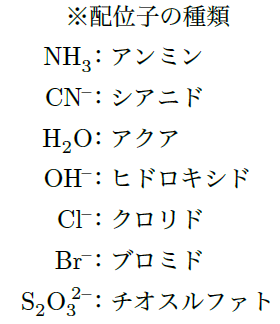
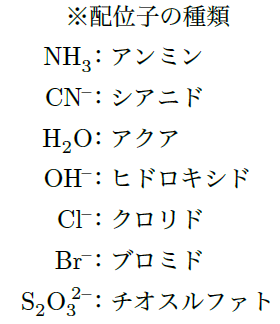



金属イオンが配位子に囲まれてできるんですね!もっと具体的にどんな錯イオンがあるんですか?



たとえば、テトラアンミン銅(II)イオン [Cu(NH₃)₄]²⁺がよく知られた錯イオンの一つだよ。これは、銅(II)イオン(Cu²⁺)がアンモニア分子(NH₃)4つと結びついてできる錯イオンだ。銅イオンが中心にあり、その周りに4つのアンモニア分子が配位結合しているんだ。この錯イオンは水溶液中で青色を示すことで知られているよ。



反応式としては、次のように表せるんだ:Cu²⁺ + 4NH₃ → [Cu(NH₃)₄]²⁺



このように、銅(II)イオンに対してアンモニア分子が4つ配位して、青いテトラアンミン銅(II)イオンができるんだよ。



青い溶液って、見たことがある気がします!錯イオンって、配位子がいくつか結びつくんですか?



そうだね。錯イオンでは、配位数という言葉が重要なんだ。配位数というのは、金属イオンに対してどれだけの配位子が結びついているかを示す数字だよ。さっきのテトラアンミン銅(II)イオンの場合、4つのアンモニア分子が結びついているから、配位数は4だね。



ほかにも、六配位錯イオンがあるよ。例えば、ヘキサアクア鉄(III)イオン [Fe(H₂O)₆]³⁺は鉄(III)イオン(Fe³⁺)が水分子(H₂O)6つと結びついてできる錯イオンなんだ。水分子が6つ配位しているから、配位数は6になるんだ。



反応式はこんな感じだよ:Fe³⁺ + 6H₂O → [Fe(H₂O)₆]³⁺



このように、水分子が鉄イオンに配位して、ヘキサアクア鉄(III)イオンができるんだ。水溶液では淡黄色を示すことが多いよ。



配位数って、錯イオンの構造を決める重要な要素なんですね!じゃあ、配位子ってどんな種類があるんですか?



配位子にはいろいろな種類があって、主に一価の配位子と多価の配位子に分けられるんだ。一価の配位子は、1つの電子対を金属イオンに提供するものだよ。さっき出てきたアンモニア(NH₃)や水(H₂O)は、一価の代表的な配位子だね。





また、錯イオンは触媒反応にも使われることが多いんだ。錯イオンを使った金属触媒は、特定の化学反応を効率よく進めるために重要な役割を果たしているんだ。たとえば、クロム錯体は有機化学の酸化反応に使われることがあるよ。
例題&解答
【例題1】
銅(II)イオン(Cu²⁺)にアンモニア(NH₃)4分子が配位してできる錯イオンの名称と化学式を示しなさい。
【解答】
銅(II)イオンにアンモニア4分子が配位してできる錯イオンの名称はテトラアンミン銅(II)イオンで、化学式は次の通りです:[Cu(NH₃)₄]²⁺
【例題2】
鉄(III)イオン(Fe³⁺)に水分子(H₂O)が6つ配位した錯イオンの名称と化学式を示しなさい。
【解答】
鉄(III)イオンに水分子6つが配位した錯イオンの名称はヘキサアクア鉄(III)イオンで、化学式は次の通りです:
[Fe(H₂O)₆]³⁺