このページのまとめ
学習のポイント
- 銀の単体は電気伝導性・熱伝導性が全ての金属の中で最大である。
- 銀は過剰のアンモニアと反応して錯イオンを形成して溶解する。
- ハロゲン化銀は感光性をもち、写真の現像に用いられる。
- ハロゲン化銀は基本的に水に溶解しないが、水溶液に対しては錯イオンを形成して溶解する場合がある。
まとめノート

このページでは,銀の性質について解説していきます。銀は原子番号47の元素で,遷移元素に分類されています。単体の反応性が低く,単体の状態で天然に産出します。ただし,酸化力がある酸とは反応するため,いくつかの化合物も形成します。今回は,銀の単体および化合物の性質について学習していきましょう。
銀の単体について

銀の単体は天然に産出し,銀白色の光沢を持っています。銀の単体は電気伝導性・熱伝導性が全ての単体の中で最大であることが知られています。しかし,高価なために一般的に電気を通すためには銅線が用いられています。銀の単体は酸化力がある酸に溶けるため,硝酸などと反応します。
銀イオンについて

銀イオンを含む水溶液に塩基を加えると,褐色の酸化銀(Ⅰ)が生じます。ここで,水酸化銀(Ⅰ)は生じないことに注意しておきましょう。また,酸化銀(Ⅰ)は過剰のアンモニアを加えると無色の錯イオンを形成して再溶解します。銀イオンがクロム酸イオンと結合して赤褐色沈殿のクロム酸銀を生じることも覚えておきましょう。
ハロゲン化銀について
写真の原理
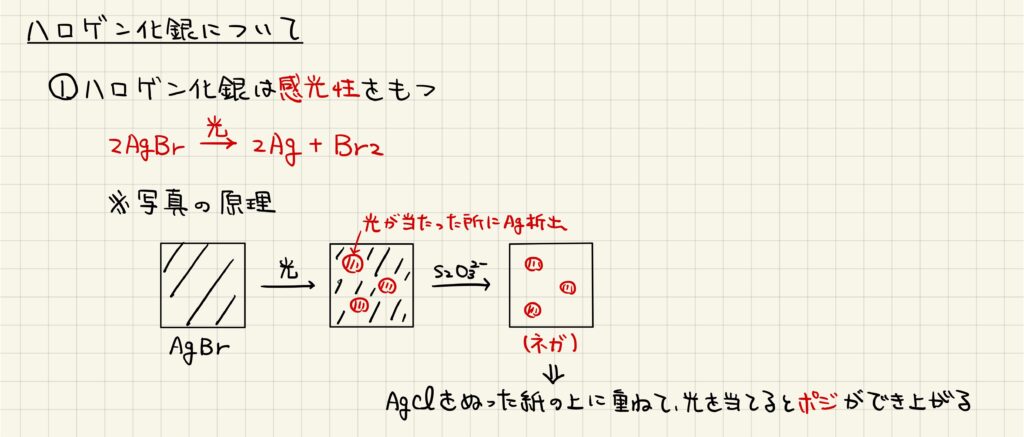
ハロゲン化銀は感光性をもち,光が当たることで銀の単体が遊離します。この性質を利用して,古くは写真の現像が行われていました。臭化銀が塗られたフィルムに光をあてることで一部に銀が析出し,残った臭化銀をチオ硫酸イオンで洗い流すことでネガが出来上がります。同様の操作を行ってネガを反転させたものがポジとなり,白黒写真を作ることができます。
ハロゲン化銀の溶解性
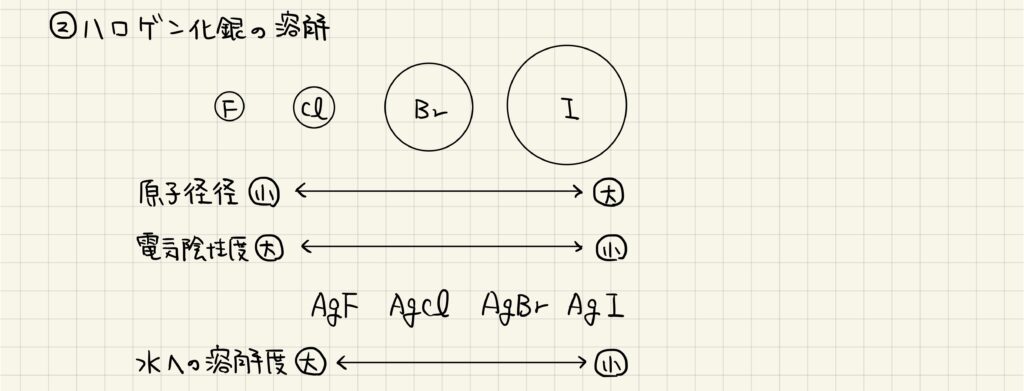
ハロゲン化銀の溶解性を考えるにあたって,ハロゲン原子の原子半径を確認しておきましょう。当然ながら,原子番号が大きくなるにつれて原子半径も大きくなっています。つまり,ヨウ素原子は最も電子を引き付ける力が弱く,銀イオンと結合した際の極性が最も小さいことになります。

ハロゲン化銀の沈殿は,それぞれ特有の色を有しています。塩化銀は白色,臭化銀が淡黄色,ヨウ化銀が黄色となります。
フッ化銀は結合の極性が非常に大きく,水に可溶です。一方,それ以外のハロゲン化銀は水に不溶となります。ただし,特定の試薬を加えることで錯イオンを形成し,沈殿を再溶解させることができます。ハロゲン化銀の種類によって再溶解させられるものが異なるので,注意して覚えておきましょう。

試薬を加えることによって錯イオンを形成し,ハロゲン化銀が再溶解します。錯イオンの名前は特殊なものもあるので,よく覚えておきましょう。