このページのまとめ
学習のポイント
- 両性元素は酸とも塩基とも反応する金属で、アルミニウム、亜鉛、スズ、鉛が代表的である。
- 金属イオンのまわりに配位子が結合してできるイオンを錯イオンと呼ぶ。
- 両性元素は、単体・酸化物・水酸化物それぞれが酸及び塩基と反応する。
まとめノート
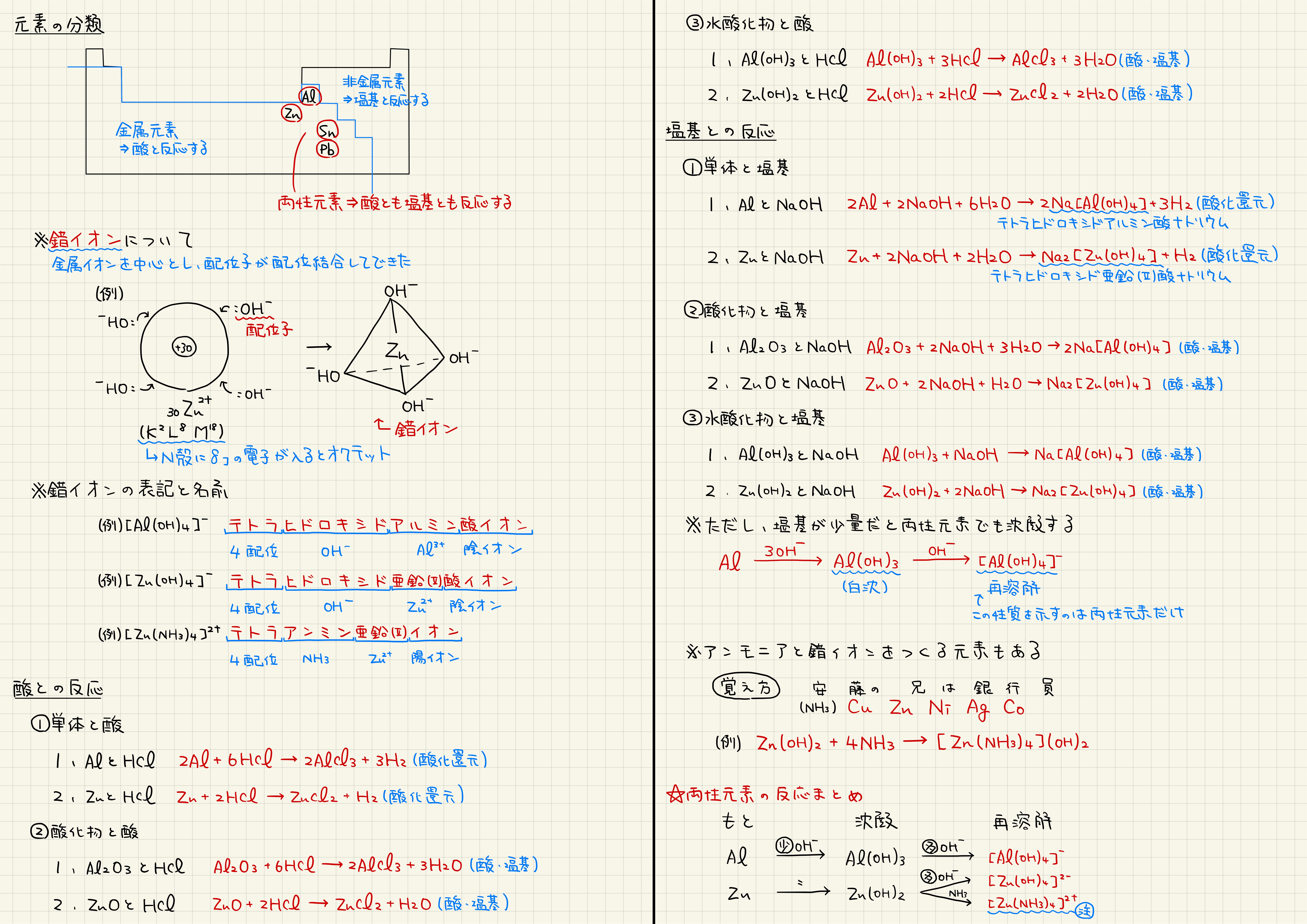
このページでは,両性元素の反応性について解説していきます。両性元素とは,単体・酸化物・水酸化物それぞれが酸とも塩基とも反応して溶解する元素を指します。高校化学の範囲では,アルミニウム,亜鉛,スズ,鉛を覚えておけば良いでしょう。反応性は三価の陽イオンになるアルミニウムと二価の陽イオンになるその他の元素とに区別されます。それぞれの反応式は必ず覚えておきましょう。
両性元素の概論
元素の分類
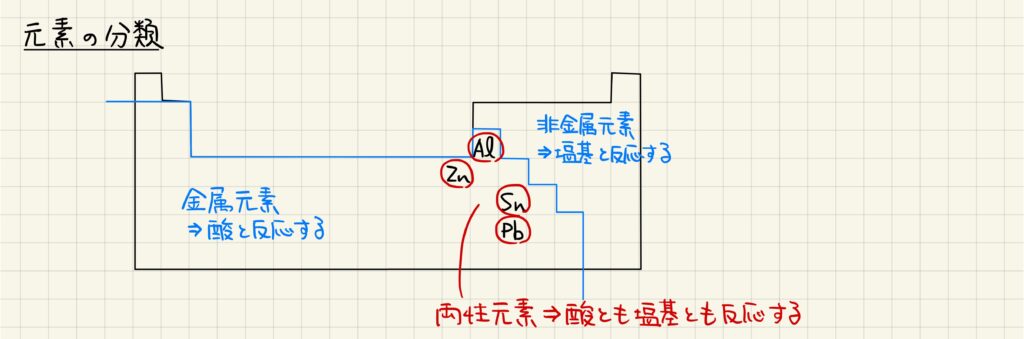
元素は,一般に金属元素と非金属元素に分類されます。金属の酸化物は塩基性酸化物と呼ばれることから,主に酸と反応します。一方,非金属の酸化物は酸性酸化物と呼ばれ,主に塩基と反応します。金属元素の中で一部塩基とも反応するものがあり,これらを総称して両性元素と呼びます。高校化学の範囲では,アルミニウム,亜鉛,スズ,鉛を覚えておきましょう。
錯イオンについて
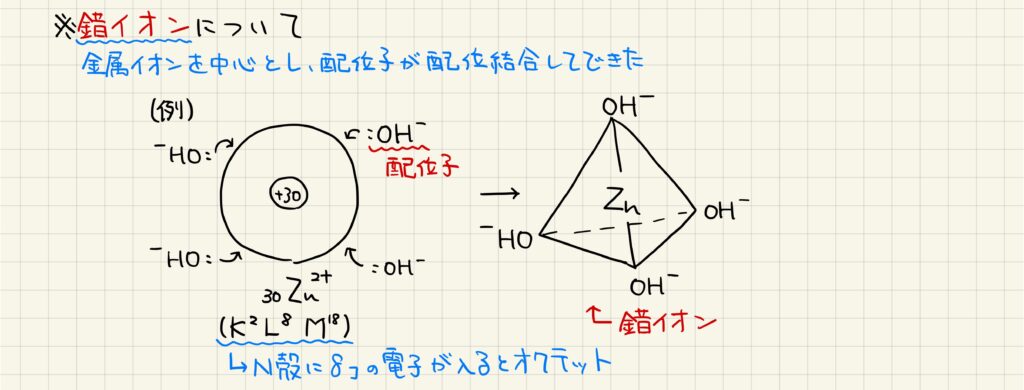
両性元素の反応では,錯イオンが形成されることがあります。錯イオンとは,金属イオンの周囲に,配位子と呼ばれる非共有電子対をもつ物質が配位結合して形成されたイオンです。例えば亜鉛イオンの周囲には4つの配位子が結合することが知られています。
錯イオンの表記と名前
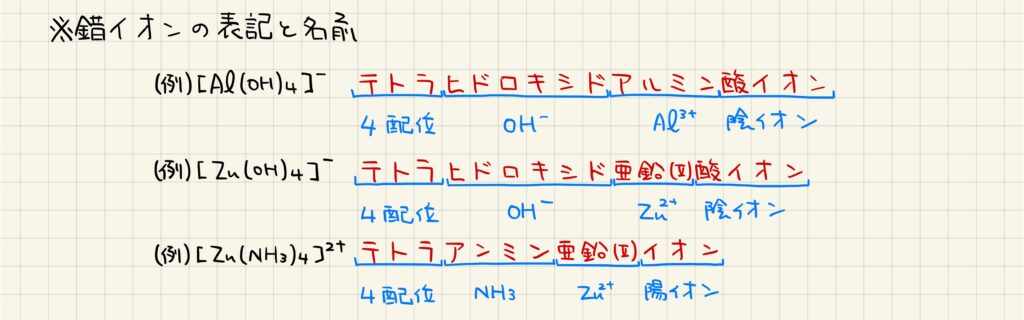
錯イオンは,名称がやや長くなります。詳しくは別の記事で解説していますので,今回は上記の3つだけ覚えておきましょう。錯イオンの名称は,配位数・配位子・中心金属イオン・イオン区別の順に呼びます。意味を捉えながら覚えていきましょう。
両性元素の反応
酸との反応

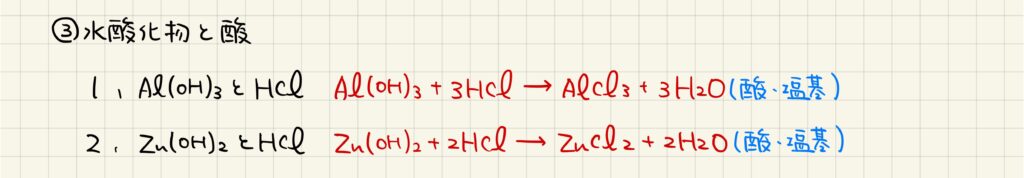
両性元素の単体・酸化物・水酸化物が酸と反応する時の化学反応式です。単体が反応するときは酸化還元反応が生じ,水素の単体が得られます。酸化物および水酸化物が反応するときは中和反応として理解することができ,塩と水が得られます。
塩基との反応

両性元素の単体・酸化物・水酸化物が塩基と反応するときの化学反応式です。酸の場合と同じで,単体との反応は酸化還元反応,それ以外の反応は中和反応として理解することができます。アルミニウムが反応したときはテトラヒドロキシドアルミン酸ナトリウム,亜鉛が反応したときはテトラヒドロキシド亜鉛(Ⅱ)酸ナトリウムが得られます。
両性元素の沈殿形成

両性元素は酸とも塩基とも反応して溶解しますが,少量の塩基と反応した場合には沈殿が生じます。アルミニウムの場合は,水酸化アルミニウムが水に不溶な白色沈殿となります。
また,両性元素とは別にアンモニアと錯イオンを形成する元素があります。銅・亜鉛・ニッケル・銀・コバルトなどが知られています。例えば亜鉛は過剰のアンモニアと錯イオンを形成し,テトラアンミン亜鉛(Ⅱ)水酸化物を形成して水に溶解します。
両性元素の反応まとめ
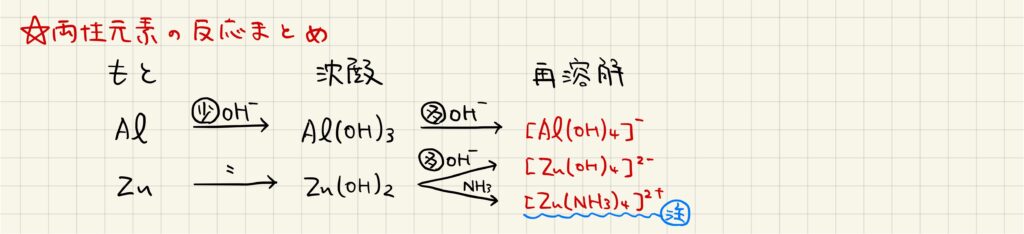
ここまで学習した反応を整理しておきましょう。アルミニウム・亜鉛ともに少量の塩基と反応した場合は沈殿を形成します。水酸化アルミニウムに対して過剰な塩基を加えた場合には錯イオンを形成して溶解します。水酸化物亜鉛には,過剰な塩基だけではなく過剰なアンモニアを加えた場合も錯イオンを形成して溶解します。