このページのまとめ
学習のポイント
- アルカリ土類金属の単体は還元剤として働き、原子番号が大きくなると還元力が強くなる。
- アルカリ金属やアルカリ土類金属のイオンを含む水溶液は炎色反応を示す。
- 硫酸カルシウムは石膏と呼ばれ、塑像や医療用ギプスなどに用いられる。
- 水酸化カルシウムと塩素からさらし粉が得られ、さらし粉は酸化剤として働く。
まとめノート

このページでは,アルカリ土類金属の性質について解説します。アルカリ土類金属とは,元素周期表の第2族元素の総称(旧課程ではベリリウムとマグネシウムを除く)です。アルカリ土類金属の原子は最外殻に2つの電子を持つため,それらを放出して二価の陽イオンになりやすいです。化合物ではカルシウムを用いたものがよく知られているため,順に学習していきましょう。
アルカリ土類金属の単体
概論
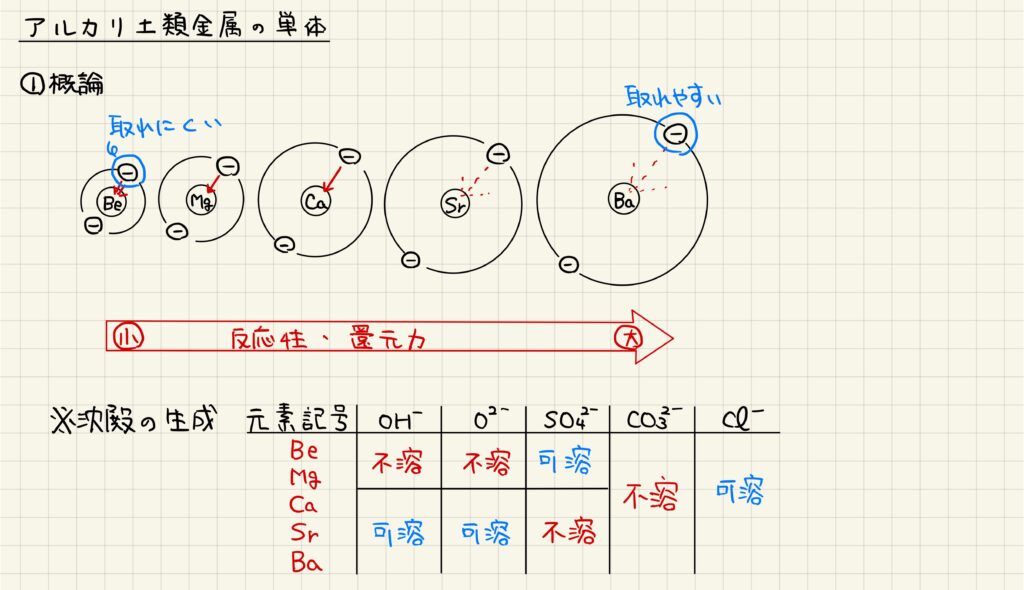
アルカリ土類金属の単体は電子を放出して陽イオンになるため,還元剤として働きます。原子半径が大きいほど電子を引き付ける力が弱いため,還元力が強くなります。一方,アルカリ金属と同様に,融点・沸点やイオン化エネルギーは原子番号が小さいほど高くなります。
アルカリ土類金属の陽イオンは,様々な陰イオンと結合して沈殿を形成します。ただし,ベリリウム・マグネシウムとそれ以外の物質とで沈殿の生成に関する法則が異なっており,注意が必要です。
反応性

アルカリ土類金属の単体は,反応性はアルカリ金属には劣りますが還元剤として働きます。空気中の酸素と反応すると,酸化物を生成します。水との反応は,元素によって異なります。ベリリウムは水と反応せず,マグネシウムは熱水と反応して弱塩基を生じます。それ以外の単体は冷水とでも反応して,強塩基を生じます。
炎色反応

アルカリ金属やアルカリ土類金属のイオンは,炎色反応により検出することができます。炎色反応とは,特定のイオンを含む水溶液に白金線を浸し,その白金線を炎の外炎にかざすことで炎に色が付く現象です。イオンと炎の色の組み合わせを覚えておきましょう。
カルシウムの化合物:セッコウ
焼きセッコウ

セッコウは,硫酸カルシウム二水和物を主成分とする物質です。セッコウを加熱することで水和水が一部失われ,焼きセッコウが得られます。この反応は可逆的なもので,焼きセッコウに水を加えてこねることでセッコウになり,固まります。このような性質を利用して,塑像や医療用ギプスがつくられています。
硬セッコウ

焼きセッコウをさらに加熱することで,硫酸カルシウム無水和物を主成分とする硬セッコウが得られます。この反応は不可逆的で,硬セッコウに水を加えても焼きセッコウには戻りません。硬セッコウはチョークやセメントの材料として利用されています。
カルシウムの化合物:さらし粉
製法

カルシウムを含む化合物として,さらし粉が知られています。さらし粉は石灰水に塩素の気体を通じることで生成されます。さらし粉は塩化物イオンと次亜塩素酸イオンという複数の陰イオンを含むため,複塩に分類されます。
性質

さらし粉に希塩酸を加えることで,塩素の単体が得られます。この時,反応物は濃塩酸ではなく希塩酸が用いられるので注意しておきましょう。また,さらし粉に含まれる次亜塩素酸イオンは酸化剤として働き,殺菌・漂白作用を示します。酸化剤として働く時の半反応式を覚えておきましょう。