このページのまとめ
学習のポイント
- ケイ素の単体は二酸化ケイ素を還元することによって得られる。
- 二酸化ケイ素はガラスの主成分として知られており、フッ化水素・フッ化水素酸・水酸化ナトリウム・炭酸ナトリウムによって浸食される。
- シリカゲルは二酸化ケイ素を加工することで得られ、乾燥剤として用いられる。
まとめノート

このページでは,ケイ素の性質について解説します。ケイ素は,元素周期表では第14族第3周期に属する元素で,原子番号は14です。ケイ素の単体は自然界にはあまり存在していませんが,生成すると半導体などに使われています。化合物ではガラスやシリカゲルの主成分として知られており,様々なところで私たちの生活を助けています。
ケイ素の単体
製法

ケイ素の単体は,二酸化ケイ素を還元することによって生成します。マグネシウムの単体を用いる方法はゴールドシュミット法と呼びます。工業的にはコークスで還元することが多いですが,コークスが少量の場合にはケイ素の単体が得られ,コークスが多量の場合には炭化ケイ素(カーボランダム)が生じます。
性質

ケイ素の単体は,半導体などの材料に用いられます。また,共有結合結晶をとり,結晶構造はダイヤモンドと類似しています。同様に,二酸化ケイ素も共有結合結晶をとります。
二酸化ケイ素

二酸化ケイ素はケイ砂やガラスの主成分として知られています。ガラスを溶かす物質として,気体のフッ化ケイ素,水溶液のフッ化ケイ素酸,水酸化ナトリウム,炭酸ナトリウムの四物質が知られています。気体のフッ化水素と水溶液のフッ化水素酸で反応が異なり,生成物も違うことに注意しておきましょう。
シリカゲルについて
製法

シリカゲルは,二酸化ケイ素を段階的に反応させていくことによって生成します。初めに,二酸化ケイ素を水酸化ナトリウムや炭酸ナトリウムによって溶解し,ケイ酸ナトリウムを得ます。これに水を加えることで粘性が大きな水ガラスを生成します。水ガラスに塩酸を加えることで弱酸遊離が起き,白色ゲルのケイ酸が生じます。最後に,ケイ酸を加熱して一部脱水することで,シリカゲルが得られます。
シリカゲルの分子構造
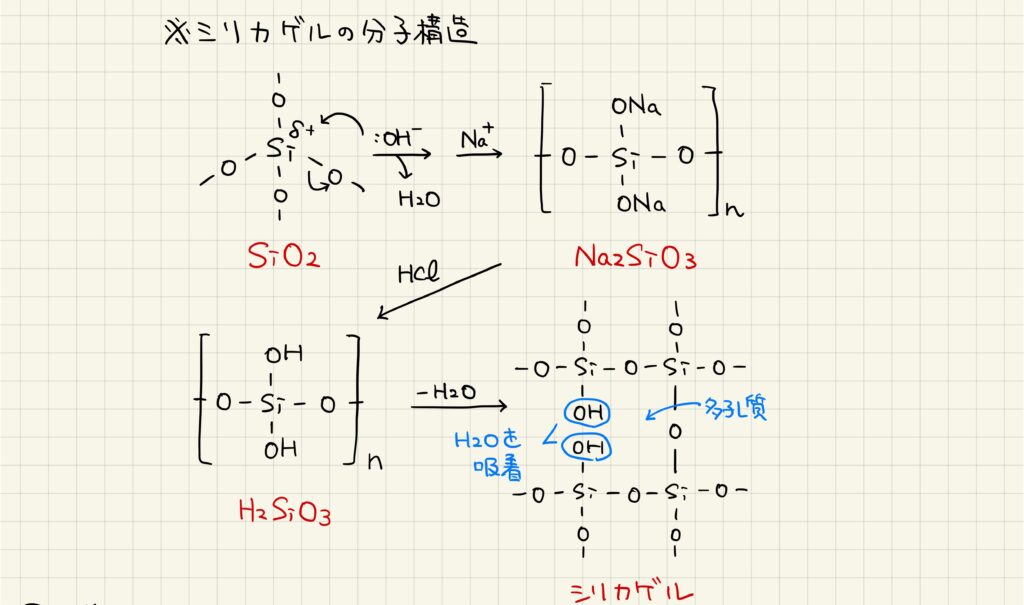
シリカゲルの分子構造を学習していきましょう。まず,二酸化ケイ素は共有結合結晶なので,正四面体方向に結合が伸びています。そこからケイ酸ナトリウムにすると一部がナトリウムで中和され,ケイ酸ではナトリウム原子が水素原子に変わります。最後に脱水することで,シリカゲルの分子構造が完成します。
性質

シリカゲルがもつヒドロキシ基が高い親水性を示し,多孔質な構造によって表面積が大きくなります。これら2つの性質によって,シリカゲルは乾燥剤として優れた働きを示します。