このページのまとめ
学習のポイント
- リンの単体は、リン鉱石・ケイ砂・コークスの混合物を加熱することで得られる。
- リンには同素体が存在し、赤リンと黄リンでは性質が大きく異なる。
- 十酸化四リンは潮解性をもち、水分とよく反応するので、乾燥剤に用いられる。
- リン酸は3価の弱酸で、肥料の原料に用いられる。
まとめノート

このページでは,リンの性質について解説をします。リンは元素周期表では第15族第3周期に属する元素で,原子番号は15です。単体には同素体が存在し,性質が大きく異なります。化合物としては十酸化四リンやリン酸が知られており,特徴的な性質を示します。
リンの単体
製法

リンの単体は,リン鉱石をケイ砂・コークスと加熱することで得られます。この反応は三つの段階に分けると理解しやすいです。一つ目は,リン鉱石の主成分であるリン酸カルシウムの熱分解によって,十酸化四リンを得ます。ここで生じた副生成物の酸化カルシウムは,二段階目でケイ砂と反応します。三段階目は,十酸化四リンをコークスで還元してリンの単体を得ます。
性質
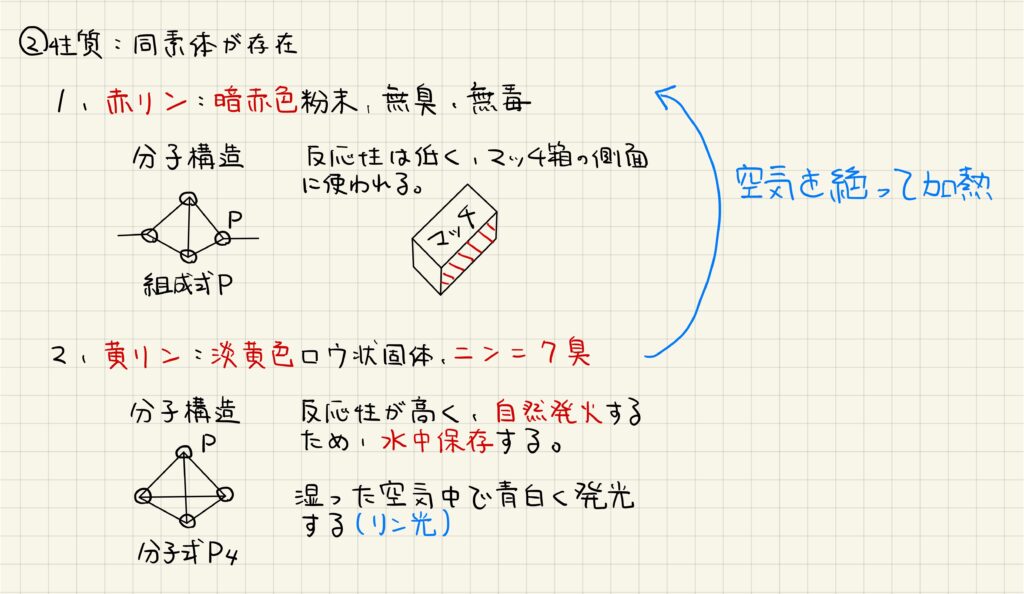
リンの単体には,同素体が存在します。赤リンは暗赤色の粉末で,無臭・無毒です。高分子の構造をとっているため,化学式はPで表されます。発火点が低く,マッチの側面に塗られています。
黄リンは淡黄色のロウ状固体で,ニンニク臭・有毒です。分子式P4で表されます。非常に反応性が高く,自然発火するために水中保存が必要です。また,湿った空気中で青白く発光し,この光をリン光と呼びます。黄リンを空気を絶って加熱することで分子構造が変わり,赤リンが得られます。
リンの化合物
十酸化四リンについて
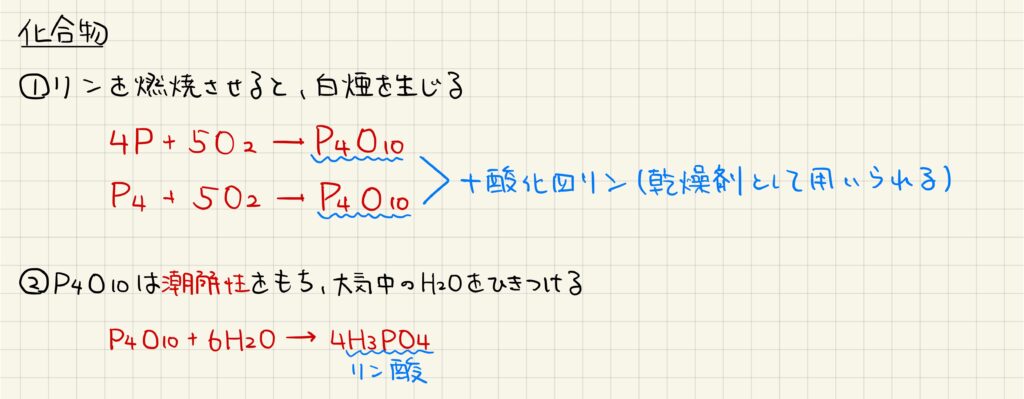
リンの単体を燃焼させると,十酸化四リンが生じ,白煙が立ちます。この十酸化四リンは潮解性をもち親水性が高いことから,乾燥剤として用いられます。水と反応するとリン酸が得られます。
リン酸について

リン酸は,三価の弱酸として働きます。それぞれの電離定数をK1,K2,K3とすると,リン酸水素イオン水溶液,リン酸二水素イオンの水溶液は両性電解質として水素イオン濃度を求めることができます。
リン酸カルシウムと硫酸が反応すると,リン酸二水素カルシウムと硫酸カルシウムが得られます。リン酸二水素カルシウムと硫酸カルシウムの混合物は過リン酸石灰と呼び,肥料として用いられます。肥料の三要素は窒素・リン・カルシウムが挙げられています。