このページのまとめ
学習のポイント
- 二酸化窒素は銅に濃硝酸を加えることで得られる。
- 二酸化窒素は赤褐色の気体で、冷水と反応すると硝酸と亜硝酸、温水と反応すると硝酸と一酸化窒素を生じる。
- 硝酸は工業的にはオストワルト法によって得られる。
- 硝酸は光によって分解され、生じた二酸化窒素がとけて黄褐色になる。
まとめノート

このページでは,二酸化窒素および硝酸について解説します。二酸化窒素は赤褐色の気体で,理論化学においては平衡の問題でよく扱われます。硝酸はオストワルト法によって製造され,酸化剤として使われることが多いです。前回に引き続き,窒素の化合物について学習していきましょう。
二酸化窒素について
製法

二酸化窒素は,銅に濃硝酸を加えることで生成されます。濃硝酸を用いた酸化還元反応では二酸化窒素が生じるので,還元剤は必ずしも銅である必要はありません。理論化学の酸化還元反応と関連して覚えておきましょう。
また,前回も扱いましたが,一酸化窒素を空気酸化することで二酸化窒素が得られます。一酸化窒素は非常に参加されやすく,容易に空気酸化される化合物です。この反応はオストワルト法でも用いるので,よく覚えておくましょう。
性質

二酸化窒素は赤褐色の酸性気体として知られています。水に溶けると酸を作りますが,水の温度によって少し反応が変化します。冷水と反応した場合は,硝酸と亜硝酸が生じます。一方,温水と反応した場合は硝酸と一酸化窒素が生じます。
また,二酸化窒素は四酸化二窒素と平衡を形成します。この反応は正反応が発熱反応なので,平衡系の温度を下げるとルシャトリエの原理に従って平衡が右に移動し,赤褐色が薄くなります。同様に,加圧した場合には濃度が上がって一瞬色が濃くなりますが,その後平衡が右に移動して徐々に色が薄くなります。
硝酸について
製法
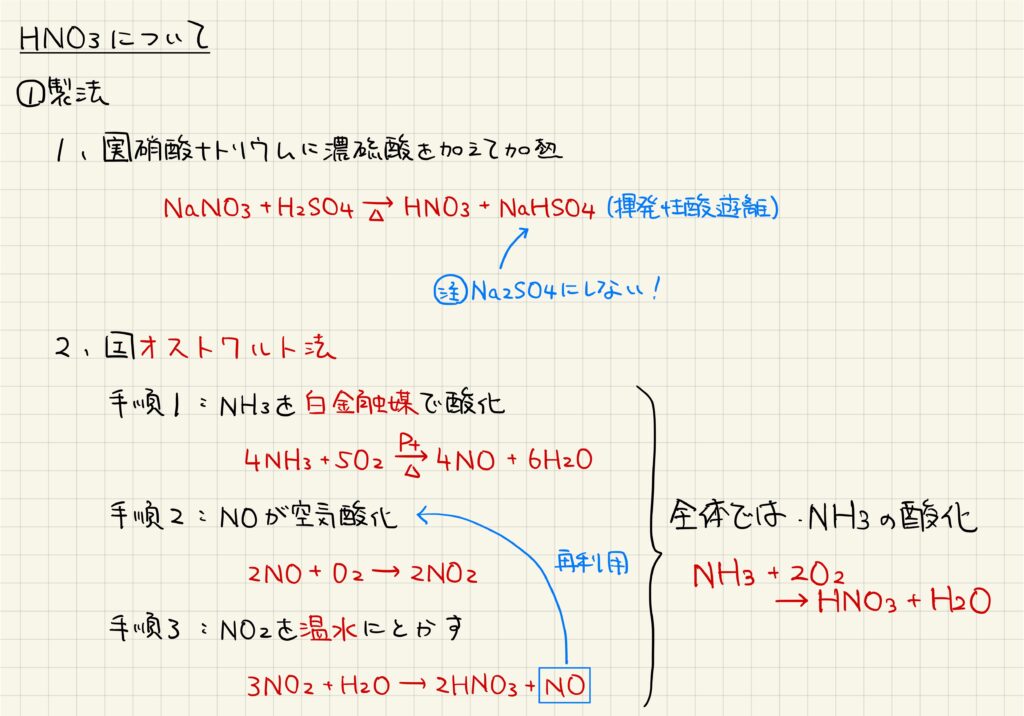
硝酸は,実験室では硝酸ナトリウムに濃硫酸を加えて加熱することで生成されます。これは揮発性酸の遊離による反応で,副生成物として硫酸水素ナトリウムが生じることがポイントです。硫酸ナトリウムは生じないので注意しておきましょう。
硝酸は、工業的には,オストワルト法によって生成されます。初めにアンモニアを白金触媒で酸化し,生じた一酸化窒素を空気酸化した後,二酸化窒素を温水に加えることで硝酸を生成します。副生成物として生じた一酸化窒素は再利用することで,無駄を省いています。この一連の反応は,アンモニアを酸化していく手順として理解できます。
性質

硝酸は,酸化力のある酸として働きます。ただし,希硝酸と濃硝酸で半反応式が異なることに注意が必要です。希硝酸からは一酸化窒素が生じ,濃硝酸からは二酸化窒素が生じます。また,金属との反応では表面に酸化被膜を作って不導体になることが知られています。
硝酸は光によって分解され,二酸化窒素が生じます。この時生じた二酸化窒素が硝酸に溶け込んで,黄褐色になります。保存方法として,光が当たらないようにするために褐色ビンで保存します。