このページのまとめ
学習のポイント
- 水素はイオン化傾向の小さい金属に希酸を加えることで生成できる。
- 水素は還元剤として働き、酸素と爆発的に反応する。
- 希ガスは第18族に分類される元素で、単原子で閉殻構造またはオクテットの状態をとり、非常に安定な電子配置である。
- 希ガスはほとんど反応しないため、価電子数は0個とする。
まとめノート
このページでは,水素および希ガスについて解説していきます。水素は原子番号1番の元素で,最も簡単な原子構造をしています。単体としてH2が存在し,様々な性質を示しています。一方,貴ガスは元素周期表の第18族に分類される元素の総称で,非常に安定な原子として存在しています。無機化学の手始めとして,これらの物質について学んでいきましょう。
【水素】H2の製法と性質について理解する
H2の製法
無機化学における製法は,実験室的製法と工業的製法とに分けられます。実験室的製法では,比較的小規模な実験装置を用いて,穏やかな条件で反応させて物質を生成します。一方,工業的製法では,大規模な実験装置を用いたり,高温高圧といった激しい条件で反応させたりして物質を生成します。どちらの製法も化学反応の反応機構から理解しておくと良いでしょう。
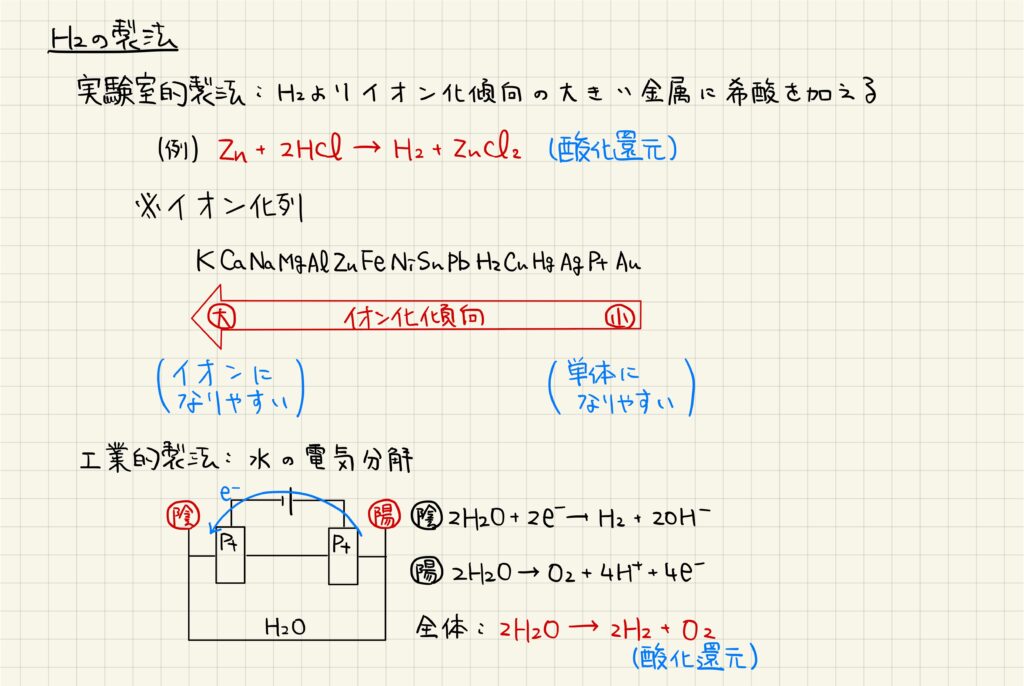
H2は,実験室ではイオン化傾向が大きい金属に希酸を加えることで生成します。ここで,イオン化傾向とは,「金属(または水素)の陽イオンへのなりやすさ」を示す指標です。主な金属をイオン化傾向順に並べたものをイオン化列と呼び,画像の通りとなります。イオン化傾向が大きい金属は電子を放出して酸化されやすい一方,水素は電子を受け取って還元されやすいです。したがって,金属と水素イオンの酸化還元反応から,水素分子を生成することができます。
工業的には,水の電気分解によってH2を生成することができます。陰極では外部電源によって電子が与えられ,水分子が還元されて水素分子が生成されます。一方,陽極では外部電源によって水分子が酸化されて酸素分子が生成されます。
H2の性質
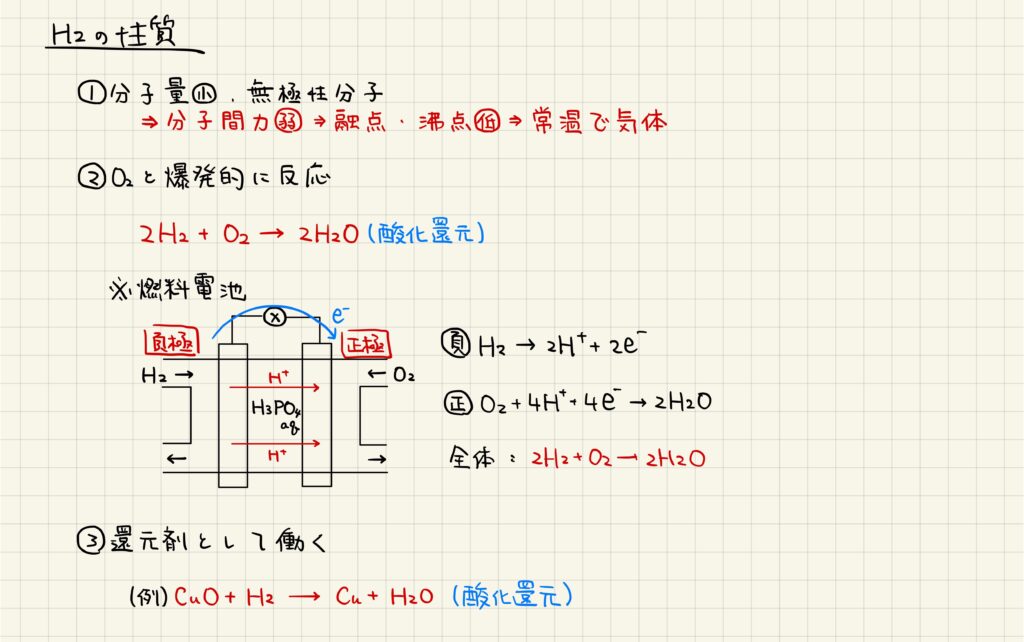
H2は,非常に分子量が小さな分子です。また,結合に極性がなく,全体で無極性分子に分類されます。分子間力の強さは分子量・分子の表面積・分子の極性にしたがって変化しますから,H2は分子間力が非常に小さいと判断することができます。分子間力が小さいために融点・沸点はかなり低く,常温で気体として存在します。
H2は,O2と爆発的に反応することが知られています。H2の還元力とO2の酸化力により,反応はかなり速く進行します。また,この反応のエネルギーを電気として取り出す装置が,燃料電池です。燃料電池の負極ではH2が酸化されて電子を放出し,正極ではO2が還元されて電子を受け取ります。全体の反応式を見れば,燃料電池が水素の燃焼反応を基にしていることがよく分かります。
最後に,H2は還元剤として働きます。例えば,金属の酸化物に対して高温高圧の水素を作用させることで酸化還元反応が進行して,金属の単体が得られることが知られています。このような反応は接触還元とも呼ばれ,単体金属の製法の一つです。
【貴ガス】安定な電子配置をしており,固有の性質を示す
貴ガスとは
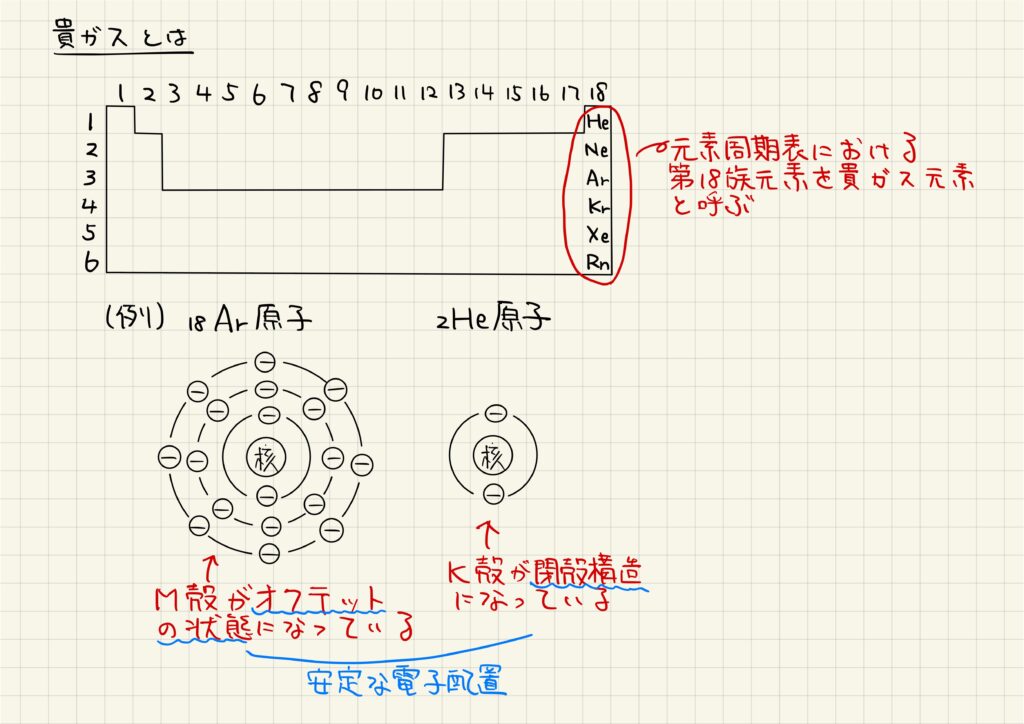
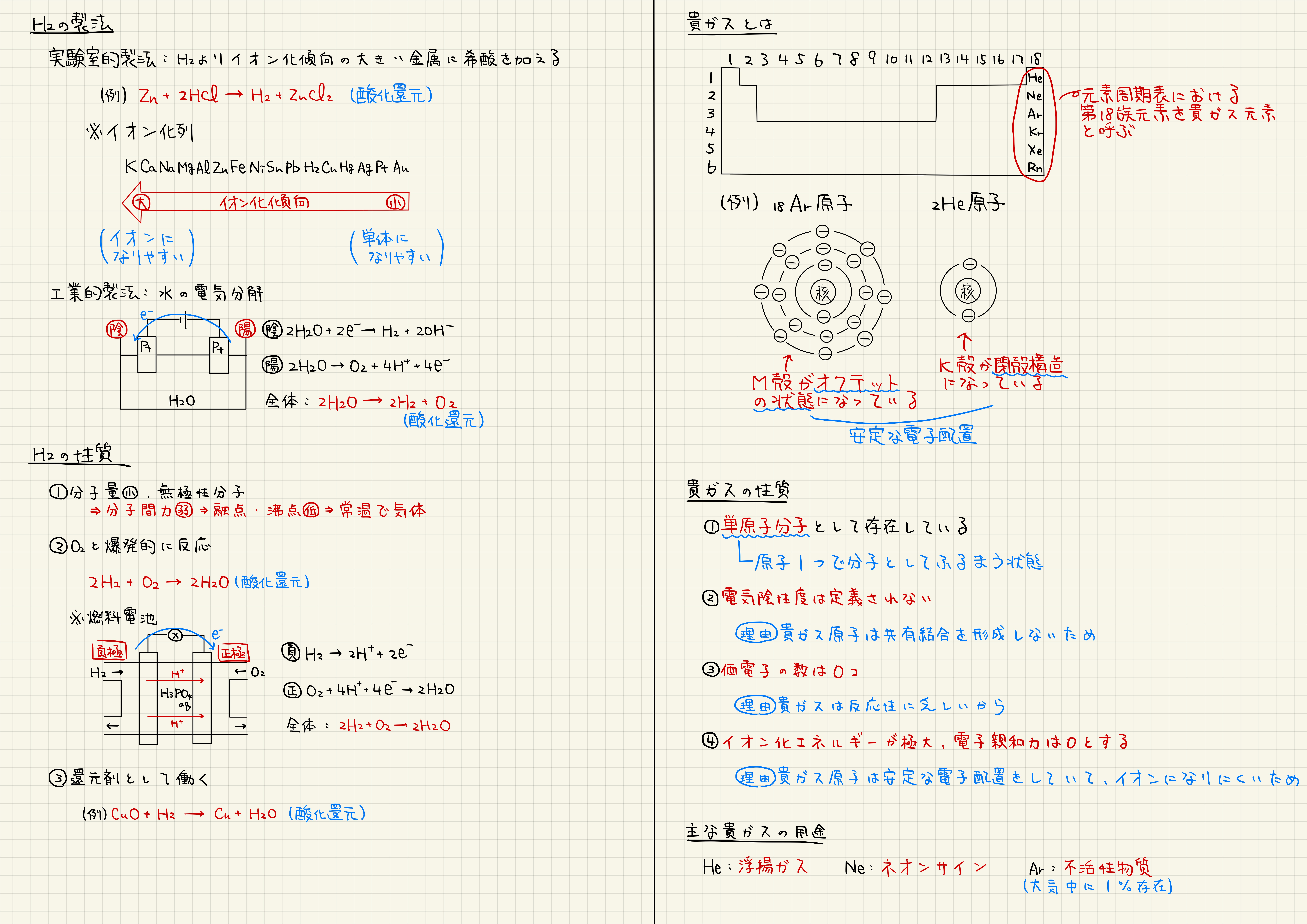
貴ガス(過去には希ガスと表記されていましたが,現在では貴ガス表記が一般化しつつあります)は,元素周期表における第18族元素の総称です。具体的には,ヘリウムHe,ネオンNe,アルゴンAr,クリプトンKr,キセノンXe,ラドンRnの6元素が該当します。これらの原子は閉殻構造またはオクテットの状態という電子配置をとっており,非常に安定な構造をしています。
貴ガスの性質

貴ガスは非常に安定な原子を形成しており,その安定性から様々な性質を示します。まず,貴ガスは単原子分子として存在することが知られています。単原子分子とは原子1つで分子として振る舞う状態であり,これは貴ガス原子が非常に安定で,他の原子と結合を形成しないことに起因しています。
先述したように貴ガスは共有結合を形成しないので,電気陰性度が定義されません。電気陰性度とは,共有電子対を引き付ける力の強さでした。ここで注意しなければならないのは,貴ガスの電気陰性度は0ではありません。「定義されない」という点が特殊なので,気を付けておきましょう。
さらに,貴ガス原子は価電子の数が0個になります。価電子とは,反応に使用される最外殻電子のことでした。貴ガスは非常に安定で反応を生じないので,価電子数が0になるという訳です。
最後に,希ガス原子のイオン化エネルギーが極大,電子親和力は0になります。イオン化エネルギーとは原子が陽イオンになるときに必要なエネルギー,電子親和力とは原子が陰イオンになるときに放出するエネルギーでした。イオン化エネルギーが大きいほど,電子親和力が大きいほどイオンになりにくいです。貴ガス原子はもともと安定な電子配置をとっているので,電子の授受によりイオンになることは非常に難しいです。したがって,イオン化エネルギーは大きく,電子親和力は小さくなります。
主な貴ガスの用途

貴ガスはいずれも大気中に微量含まれており,様々な場面で使われています。ヘリウムガスは非常に軽いという特性を活かして,風船や気球のための浮揚ガスとして用いられます。実際にはH2の方が軽いのですが,安定性を考慮してヘリウムガスが使われることが一般的です。他にも,ネオンガスがネオンサインに用いられたり,アルゴンガスは不活性物質として用いられることがあります。これらはいずれも貴ガスの安定性を活用した事例と捉えることができます。